Nemetali, metali, soli i kemijski račun
1.1.Nemetali, oksidi nemetala i kiseline
Dušik i kisik

Tekući dušik koristi se za čuvanje bioloških uzoraka.

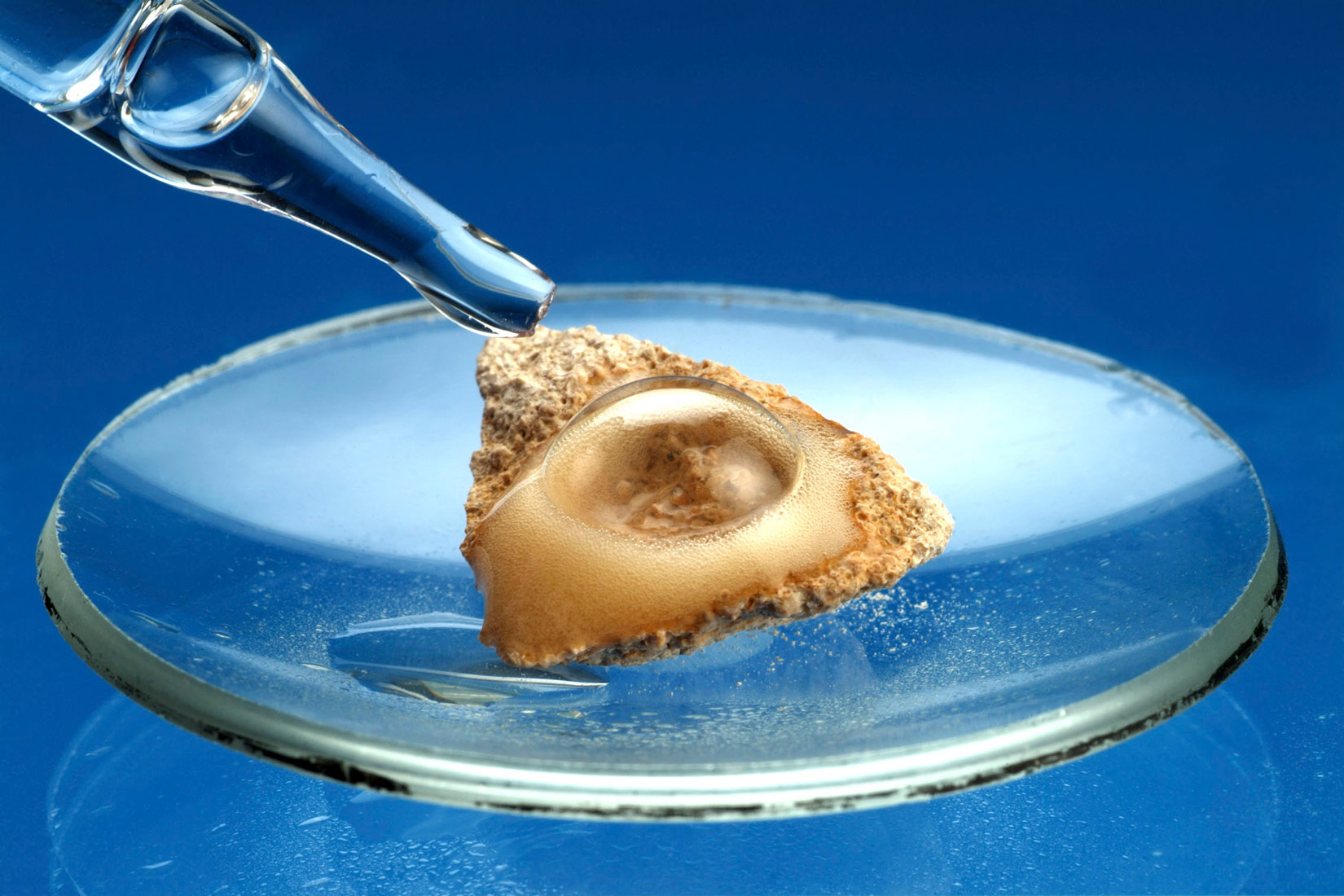
Tekući kisik u Dewarovoj tikvici
(Vakuumska tikvica, Dewarova tikvica ili termos-boca izolacijska je posuda za pohranu tvari koja produljuje vrijeme tijekom kojeg sadržaj boce ostaje topliji ili hladniji od okoline. Posudu je izumio sir James Dewar 1892. godine.)
1.2.Metali, oksidi metala i baze
Metali koje možemo rezati nožem!

U skupinu alkalijskih metala ubrajamo litij, kalij, natrij, rubidij, cezij i francij. Litij, natrij i kalij čuvamo u petroleju ili u parafinskom ulju.

Ti su metali srebrnosive boje, gustoća im je mala i možemo ih rezati nožem.

Alkalijski su metali reaktivni, izloženi zraku mogu se zapaliti, a s vodom burno reagiraju. Slika prikazuje reakciju natrija i vode.

Plamen će promijeniti boju ako se u njega unese vodena otopina soli alkalijskih metala. Vodena otopina litija oboji plamen crveno.

Vodena otopina natrija oboji plamen žuto.

Vodena otopina kalija oboji plamen ljubičasto.
Svojstva metala
Indikatori kojima dokazujemo lužine

Univerzalni indikator mijenja boju u lužinama iz žute u zelenu ako je lužina slaba. U jakoj lužini boja će se promijeniti iz žute u plavu. Odgovarajuće pH-vrijednosti za lužine mogu biti od 8 do 14.

Karakteristični je indikator za lužine fenolftalein. Indikator pripremljen kao tekućina nema boje, a u dodiru s lužinom mijenja boju u purpurnu (boja cikle). Nijansa boje varira od nježnoružičaste do intenzivnopurpurne ovisno o jakosti lužine.

Metiloranž u lužinama mijenja boju iz narančaste u žutu.

Sok crvenog kupusa, kao prirodni indikator, u lužinama mijenja boju iz ljubičaste u zelenu ako je lužina slaba, a iz ljubičaste u žutu ako je lužina jaka.