Bjelančevine
- prikazati opću strukturnu formulu aminokiselina
- klasificirati nazive i strukturne formule nekoliko jednostavnih aminokiselina
- objasniti nastajanje molekula dipeptida i oligopeptida
- poznavati izvore esencijalnih aminokiselina
- komentirati nužnost unosa bjelančevina kao izvora energije i kao gradbenih komponenata organizma
- opisati i objasniti fizikalna i kemijska svojstva bjelančevina te njihovu biološku ulogu
- protumačiti razliku između primarne i sekundarne strukture bjelančevine.
Uvod
Inzulin
Šećerna bolest ili dijabetes jest poremećaj pri kojemu gušterača proizvodi premalo inzulina.
Inzulin je hormon koji je potreban da bi šećer ušao u stanice koje proizvode energiju.
Brojni su znanstvenici dugi niz godina istraživali povezanost gušterače i šećerne bolesti.
Trebalo je proći oko 120 godina od Paula Langerhansa, koji je proučavao strukturu gušterače mikroskopom, pa do komercijalne prodaje sintetičkog humanog inzulina – lijeka koji danas pomaže milijunima ljudi oboljelih od šećerne bolesti.
Inzulin je peptid koji se sastoji od pedeset i jedne (51) aminokiseline.
Izgrađen je od dvaju međusobno povezanih lanaca i prvi je peptid kojemu je određen točan redoslijed aminokiselina.
Za to je otkriće Frederick Sanger 1958. godine dobio Nobelovu nagradu.
Uvod
Trebalo je proći oko 120 godina od Paula Langerhansa, koji je proučavao strukturu gušterače mikroskopom, pa do komercijalne prodaje sintetičkog humanog inzulina. Tijekom tih godina u rješavanju povezanosti između gušterače i šećerne bolesti sudjelovali su brojni znanstvenici.
Inzulin je peptid koji se sastoji od pedeset i jedne (51) aminokiseline. Izgrađen je od dvaju međusobno povezanih lanaca i prvi je peptid kojem je određen točan redoslijed aminokiselina. Za to je otkriće Frederick Sanger 1958. godine dobio Nobelovu nagradu.
Prvi je put inzulin korišten u liječenju šećerne bolesti 1922. godine u Torontu. Od tada pa do danas inzulin spašava brojne ljudske živote.
Bjelančevine ili proteini
Bjelančevine ili proteini (grč. protos = prvi) biološki su važni organski spojevi.
Izgradnja tijela, imunitet, prijenos plinova, biokatalizatori, hormoni – samo su neke od važnih uloga bjelančevina u organizmu živih bića.
Bjelančevine nastaju međusobnim spajanjem velikog broja aminokiselina.
Sastoje od ugljika, vodika, kisika i dušika.
Osim navedenih, u sastavu pojedinih bjelančevina može biti i drugih kemijskih elemenata.
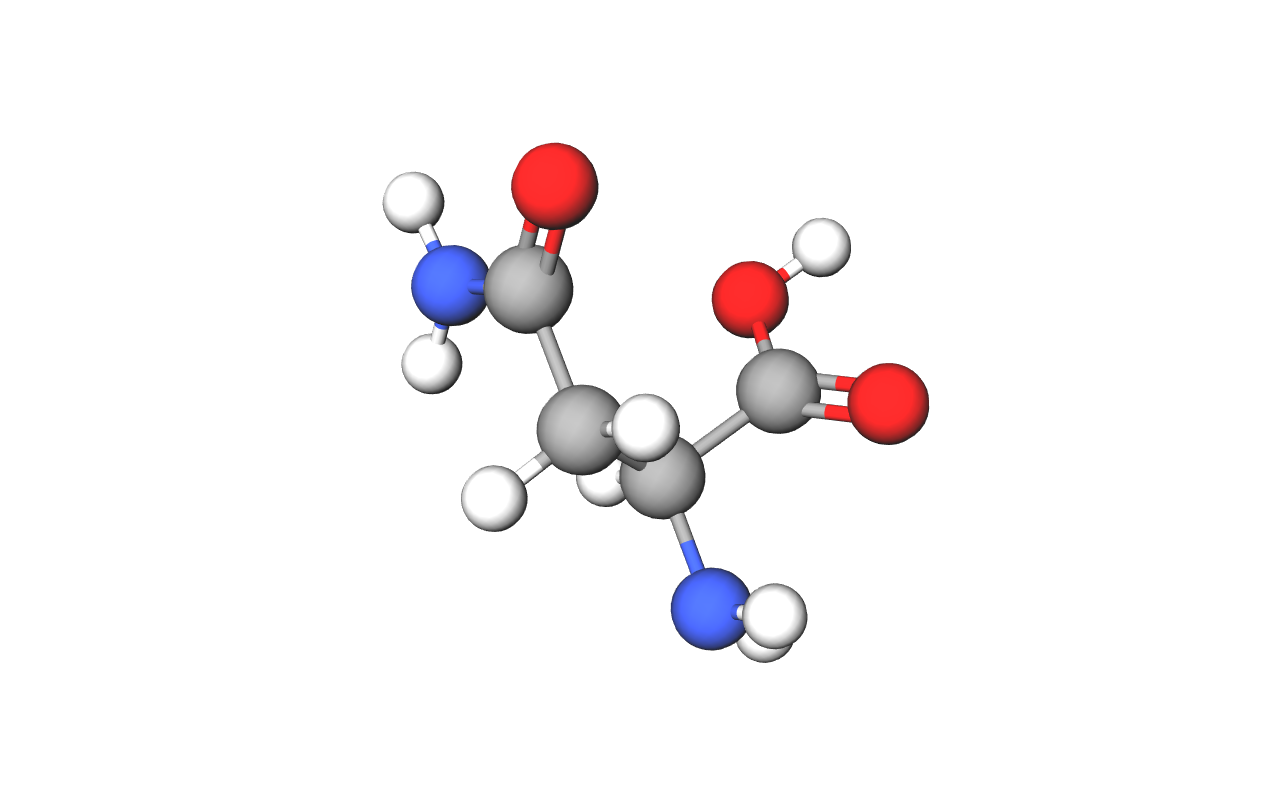
Aminokiseline su organske kiseline koje sadrže:
- karboksilnu funkcijsku skupinu () i
- amino skupinu ().
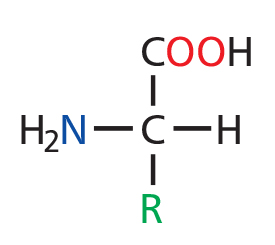
Građu aminokiseline možemo prikazati općom formulom:
.
Bjelančevine ili proteini
Bjelančevine ili proteini (grč. protos = prvi) biološki su važni organski spojevi s brojnim različitim funkcijama. Izgradnja tijela, imunitet, prijenos plinova, biokatalizatori, hormoni – samo su neke od važnih uloga bjelančevine u organizmu živih bića.
Prema svojoj građi bjelančevine su prirodne polimerne tvari koje nastaju međusobnim spajanjem velikog broja aminokiselina. Bjelančevine se sastoje od ugljika, vodika, kisika i dušika. Osim navedenih, u sastavu pojedinih bjelančevina može biti i drugih kemijskih elemenata.
Aminokiseline su organske kiseline koje uz karboksilnu funkcijsku skupinu, (), sadrže još i amino skupinu, ().
Građu aminokiseline možemo prikazati općom formulom:
Međusobne razlike između pojedinih aminokiselina odnose se na bočni ogranak označen slovom “R” u općoj formuli.
Položaj amino skupine u molekuli je na drugom ugljiku, odmah poslije karboksilne skupine. Zato te molekule nazivamo 2-aminokiseline ili još alfa-aminokiseline.
Neke α-aminokiseline sintetiziraju se u organizmu, ali se, primjerice, β-aminokiseline ne mogu stvoriti.
Zanimljivo je istaknuti da od stotinjak poznatih prirodnih aminokiselina, samo njih dvadeset (20) sudjeluje u izgradnji bjelančevina.
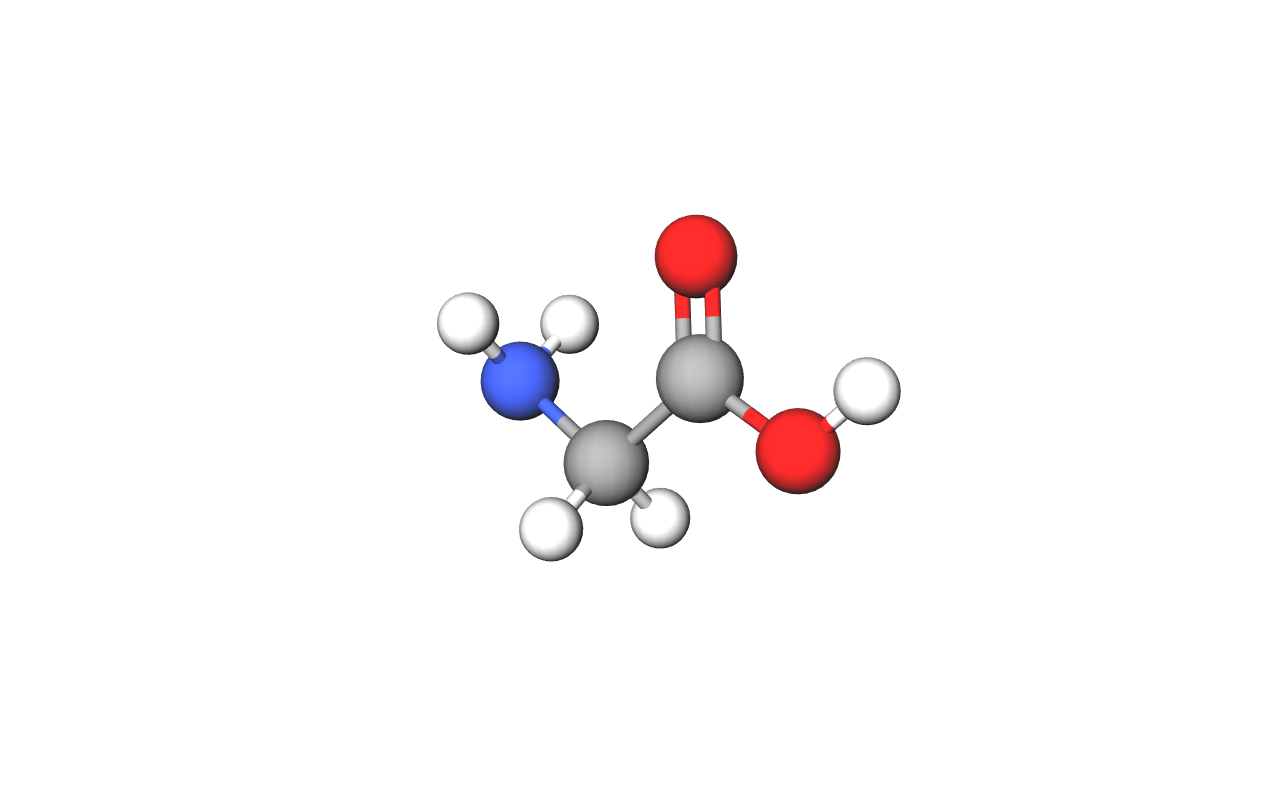
Glicin, najjednostavnija aminokiselina, na mjestu bočnog ogranka ima atom vodika.
U bočnom ogranku aminokiseline može biti ugljikovodični dio molekule različite duljine i građe, a može sadržavati i još neku funkcijsku skupinu.
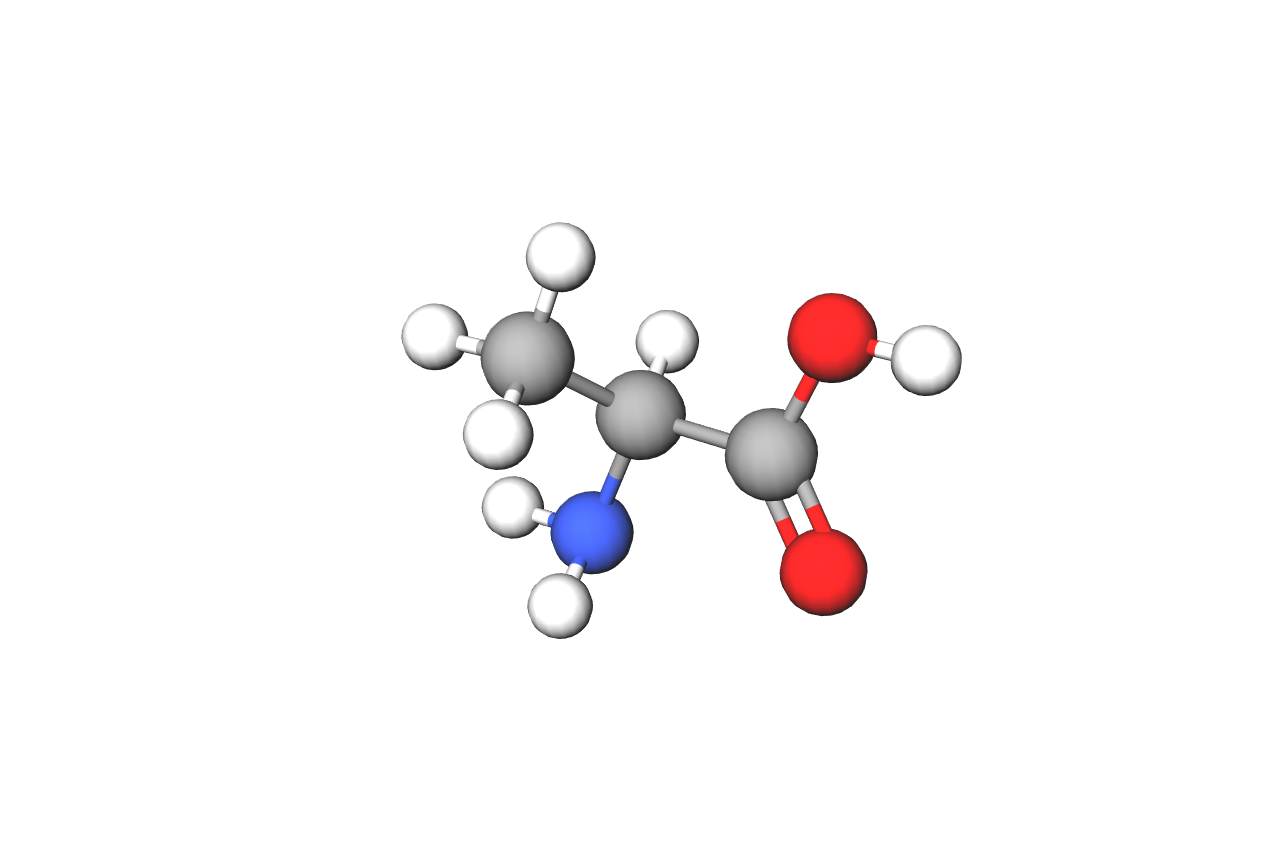
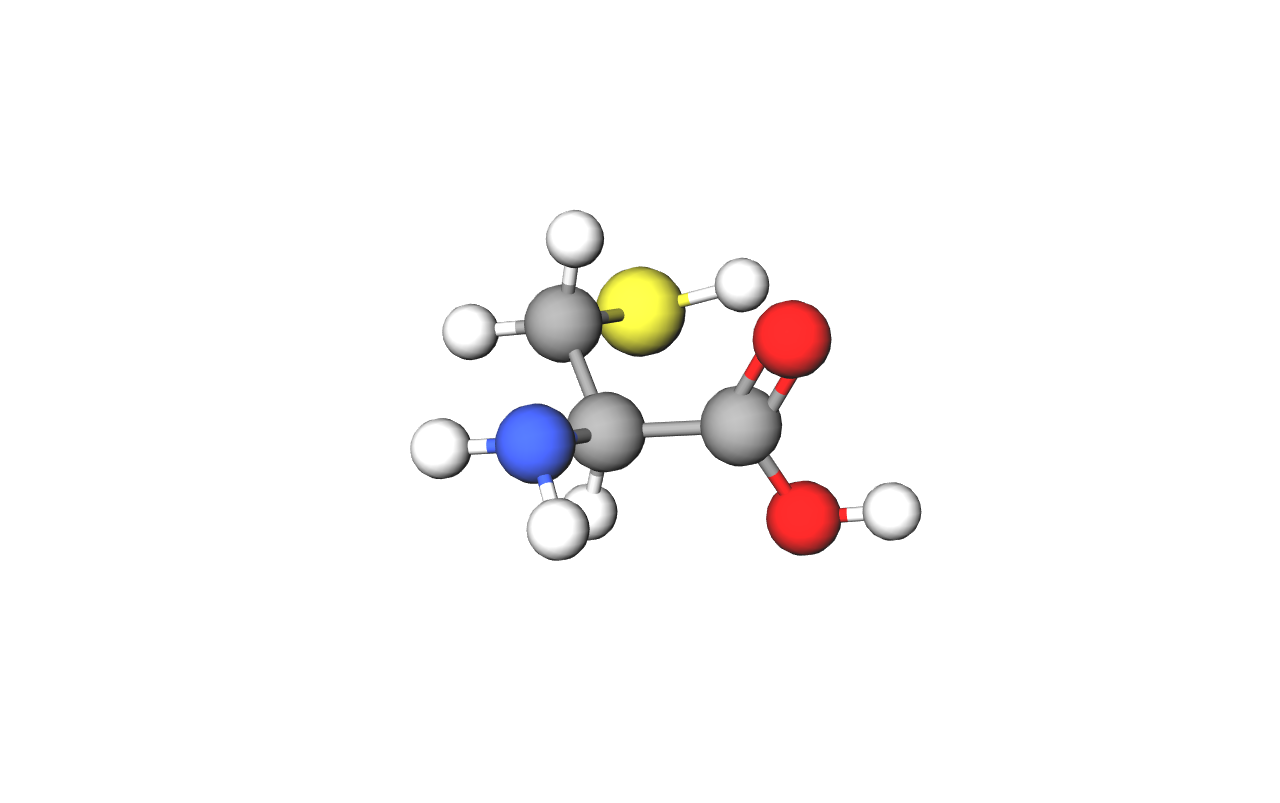
Sljedeća tablica prikazuje naziv i sažetu strukturnu formulu triju aminokiselina. Osim punim imenima, uobičajeno je aminokiseline označavati i kraticama.
Svojstva aminokiselina
Pri sobnoj temperaturi aminokiseline su većinom čvrste tvari bijele boje.
Imaju visoka tališta i topljive su u vodi.
U svojoj strukturi imaju i kiselinsku (-COOH) i bazičnu (-NH2) funkcijsku skupinu.
To znači da aminokiseline imaju svojstva i kiselina i baza, stoga kažemo da su aminokiseline amfoterne.
Svojstva aminokiselina
Pri sobnoj temperaturi aminokiseline su većinom čvrste tvari bijele boje. Imaju visoka tališta i topljive su u vodi. S obzirom na to da u svojoj strukturi imaju i kiselinsku, (), i bazičnu, (), funkcijsku skupinu, aminokiseline imaju amfoterna svojstva.
Aminokiseline i prehrana
U svojemu organizmu ljudi ne mogu sintetizirati sve potrebne aminokiseline i zato ih se mora unositi u tijelo putem hrane. Takve aminokiseline nazivamo esencijalnim aminokiselinama.
Namirnice bogate bjelančevinama, ujedno i esencijalnim aminokiselinama, mogu biti biljnog i životinjskog podrijetla.
Žitarice, mahunarke (grah, grašak, soja, leća) i drugo povrće, sjemenke suncokreta i orašastih plodova, meso, piletina, riba, jaja, mlijeko i mliječni proizvodi bogati su bjelančevinama.
Pri tome se treba prisjetiti piramide pravilne prehrane i pojedine namirnice koristiti u pravilnoj količini.
Istražite važnost BCAA aminokiselina (aminokiseline razgranatog lanca) u prehrani.
Osim za izgradnju tkiva i organa, bjelančevine su važne za imunitet, disanje, stvaranje hormona i enzima. Hrana bogata bjelančevinama služi i kao izvor energije za organizam. Prosječno masa od 1 g bjelančevina daje energiju od 4 kcal (16,74 kJ).
Na tržištu postoje specijalizirane kuhinjske vage koje mogu prikazati masu, količinu pojedinih hranjivih tvari i energijsku vrijednost određene namirnice. Takve su vage naročito pogodne za bolesnike ili druge osobe koje trebaju posebno kontrolirati svoju prehranu i paziti na “unos kalorija”.
Povezivanje aminokiselina
Molekule aminokiselina mogu se povezati peptidnom vezom u veće molekule koje zovemo peptidi.
Dvije aminokiseline spajaju se tako da se amino skupina jedne aminokiseline spaja s karboksilnom skupinom druge aminokiseline.
Pritom se izdvaja jedna molekula vode.
Peptidi izgrađeni od dviju aminokiseline nazivaju se dipeptidi.
Peptidi izgrađeni od triju aminokiselina nazivaju se tripeptidi, od četiriju tetrapeptidi itd.
Peptide s više od 100 aminokiselina nazivamo polipeptidi ili bjelančevine.
Povezivanje aminokiselina
Molekule aminokiselina međusobno se mogu povezati peptidnom vezom u veće molekule koje zovemo peptidi. Dvije se aminokiseline spajaju tako da se amino skupina jedne aminokiseline spaja s karboksilnom skupinom druge aminokiseline i pritom se izdvaja jedna molekula vode.
Peptidi izgrađeni od dviju aminokiselina nazivaju se dipeptidi, od triju aminokiselina tripeptidi, od četiriju tetrapeptidi itd.
Peptide od 10 aminokiselina nazivamo oligopeptidi, a one s više od 100 aminokiselina nazivamo polipeptidi ili bjelančevine.
Točan redoslijed aminokiselina u peptidnom lancu nazivamo primarnom strukturom bjelančevine.
Složenost strukture bjelančevina
Građa
Vlaknaste bjelančevine, npr. keratin i kolagen, nalaze se u sastavu kože, kose, noktiju i perja.
Kolagen čini osnovna vlakna vezivnog tkiva. Nalazi se u sastavu brojnih tkiva i organa (koža, hrskavica, tetive, očna leća i rožnica oka).
Kuglaste bjelančevine, npr. albumin, nalaze se u bjelanjku jajeta i krvnoj plazmi. Neki hormoni i enzimi također pripadaju kuglastim bjelančevinama.
Osim navedenoga, brojne bjelančevine imaju još složeniju građu. Ona se odnosi na međusobno povezivanje više peptidnih lanaca.
Hemoglobin je primjer bjelančevine koja ostvaruje složenu tercijarnu strukturu. Osim peptidnih lanaca u hemoglobinu se nalaze i kationi željeza.
Svojstva bjelančevina
Bjelančevine su vrlo osjetljive tvari. Biološki su aktivne samo pri određenoj temperaturi. Povećanjem temperature iznad 60 °C ili snižavanjem temperature ispod 0 °C narušava se struktura bjelančevina i one gube svoju funkcionalnost. Narušavanje strukture bjelančevine naziva se denaturacija.
Kod denaturacije bjelančevina vidljivo je stvaranje bijelog taloga jer dolazi do zgrušavanja (koagulacije) molekula bjelančevina.
Osim utjecaja temperature, denaturaciju i koagulaciju bjelančevina može uzrokovati dodatak jake kiseline ili lužine, otopine soli teških metala i alkohola.
Bjelančevine krvne plazme naročito su osjetljive na visoku temperaturu. Ako su duže vrijeme izložene temperaturi većoj od 42 °C, bjelančevine krvne plazme zgrušavaju se i može doći do smrtnih posljedica. Zato je iznimno važno da roditelji skrbe za malu djecu kada su bolesna i imaju povišenu temperaturu.
Povlačenjem elemenata uskladi odgovarajuće parove.
Spojite parove premještajući pojmove po stupcima.
Spojite odgovarajuće parove.
alanin
aminokiselina
kolagen
povezuje aminokiseline u bjelančevinu
koagulacija
složena bjelančevina, sadrži ione željeza
hemoglobin
bjelančevina netopljiva u vodi
peptidna veza
proces grušanja bjelančevina
Želite li pokušati ponovo?
Biuret-reakcija (testna reakcija na proteine)
Prisutnost bjelančevina u uzorku tvari može se dokazati biuret-reakcijom. Ta vrsta testne reakcije specifična je za sve spojeve koji imaju peptidnu vezu.
Reagens se sastoji od lužnate otopine bakrova(II) sulfata. Pripremi se vodena otopina bjelanjka jajeta (1 : 1). U epruvetu se nalije 2 mL otopine bjelanjka i isto toliko 20 %-tne natrijeve lužine.
Na kraju se kapne samo jedna kap razrijeđene vodene otopine bakrova(II) sulfata. Epruvetu lagano potresemo. Pojavljuje se karakteristična ljubičasta boja otopine.
Uz pomoć lužine voda hidrolizira bjelančevine na aminokiseline. Bakrovi ioni, , s aminokiselinama daju ljubičastu boju otopine. Ako se koristi prevelika količina vodene otopine bakrova(II) sulfata, nastaje plavozeleni talog bakrova(II) hidroksida zbog kojeg katkad nije vidljiva ljubičasta boja otopine.
Sastav mlijeka
Na kraju…
Riješite interaktivni kviz!
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Bjelančevine ili proteini prirodni su polimeri:
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Označite netočnu tvrdnju o proteinima.
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Aminokiseline se u peptidima međusobno povezuju:
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Biuret-reakcijom dokazujemo:
Želite li pokušati ponovo?
Više informacija o ovoj temi možete pronaći u jedinici 2.5 Proteini u DOS-u Biologija 1.