

U prošlosti se smatralo da je toplina fina termalna tvar koja nema težinu i koja tijekom zagrijavanja tijela ulazi, a tijekom hlađenja izlazi iz njega.

Benjamin Thompson (1753. – 1626.) bio je engleski fizičar i političar koji je tijekom obrade metala primijetio oslobađanje velike količine topline. Tada se smatralo da termalna tvar grije usitnjene dijelove metala i da u svakom materijalu postoji ograničena količina termalne tvari. Thompson je opovrgnuo te tvrdnje, dokazao pojavu topline bez usitnjavanja materijala i zaključio kako ne postoji ograničena termalna tvar.


James Prescott Joule konstruirao je uređaj prikazan na fotografiji.
Uteg mase visi na visini i ima potencijalnu energiju
Uteg svojom težinom okreće vreteno s lopaticama koje prolaze tekućinom i zagrijavaju je trenjem. U ovom pokusu potencijalna energija koju je imao uteg "utrošena" je na zagrijavanje tekućine. Tim pokusom Joule je odredio mehanički ekvivalent topline, odnosno vezu između mehaničkog rada i topline.
Precizna mjerenja pokazuju da energija potrebna za zagrijavanje jedne litre vode za (od do ) iznosi Ta je jedinica nazvana (kalorija). Od 31. prosinca 1980. za toplinu se više ne koristi mjerna jedinica kalorija. Mjerna jedinica kilokalorija, kcal, i danas se koristi u situacijama u kojima govorimo o kalorijskoj vrijednosti hrane i pića, bazalnom metabolizmu, energiji koju zahtijeva obavljanje neke radnje i sl.
O temperaturi možete više pročitati u jedinici 1.1. Temperatura.
Podsjetimo se da je temperatura mjera za zagrijanost tijela, odnosno mjera za srednju brzinu toplinskog gibanja molekula. Što je veća brzina gibanja molekula, viša je temperatura, i obrnuto.
Molekule u toplinskom gibanju imaju kinetičku energiju, a zbog međusobnih privlačenja, odnosno odbijanja, imaju i potencijalnu energiju. Ukupan zbroj kinetičkih i potencijalnih energija molekula nekog čvrstog tijela, tekućine ili plina naziva se unutarnja energija .
Mjerna jedinica za unutarnju energiju jest džul,
.
Stavimo li zagrijano tijelo u posudu s hladnom vodom, ona će se nakon nekog vremena zagrijati. Kažemo da je toplina prešla s tijela na vodu.
Toplina je energija koja spontano prelazi s tijela koje ima višu temperaturu na tijelo koje ima nižu temperaturu dok im se temperature ne izjednače, odnosno dok se ne izjednače njihove unutarnje energije.
Prijelaz topline odvija se među tijelima koja su u termičkom kontaktu.
Za dva tijela različitih temperatura kažemo da su u termičkom kontaktu kada između njih nema izolatora topline. Kad se temperature tijela koje su u termičkom kontaktu izjednače, tada više nema prijelaza topline.
Oznaka za toplinu je
, a mjerna jedinica džul,
.
Animacija prikazuje tri kuglice od različitih materijala koje se uranjaju u zagrijanu vodu. Pogledajte što se dogodi kad se ispuste na parafin...
Kuglice su jednakih masa i temperatura. Jesu li tijekom zagrijavanja primile jednaku količinu topline?
Koja je kuglica primila najviše topline?
Koje je različito svojstvo kuglica uvjetovalo različitu sposobnost primanja toplinske energije?
Sposobnost tijela da pohrani određenu količinu toplinske energije određena je njegovim toplinskim kapacitetom.
Vjerojatno vam je iz osobnog iskustva poznato kako je neke tvari lakše, a neke teže zagrijati, odnosno ohladiti.
Na primjer, istim izvorom topline teže je zagrijati određenu masu vode nego komad željeza jednake mase. Također, voda će se pri jednakim okolnim uvjetima sporije hladiti nego komad željeza jednake mase.
Zaključuje se da zagrijavanje tvari ovisi i o vrsti materijala od kojih su izrađene.
Eksperimentalno je dokazano da je količina topline potrebna za zagrijavanje neke tvari s temperature na temperaturu proporcionalna razlici konačne i početne temperature gdje je
Kako bismo umjesto znaka proporcionalnosti postavili znak jednakosti, potrebno je uvesti konstantu proporcionalnosti .
Konstanta proporcionalnosti u ovoj jednadžbi naziva se toplinski kapacitet.
Toplinski kapacitet kvocijent je topline dovedene tijelu i povećanja temperature koju je toplina prouzročila.
Mjerna jedinica za toplinski kapacitet jest ili
Eksperimentima i mjerenjima utvrđeno je kako se s povećanjem mase tvari povećava i toplinski kapacitet. Vjerojatno vam je poznato da je lakše postići određenu promjenu temperature zagrijavanjem manje mase neke tvari nego zagrijavanjem veće masu iste te tvari.
Slično se događa i pri hlađenju.
Konstanta
u jednadžbi
ovisi o toplinskim svojstvima tvari, ali i o masi tvari. Zato definiramo novu fizikalnu veličinu koja se naziva specifični toplinski kapacitet.
Specifični toplinski kapacitet fizikalna je veličina kojom se iskazuje koliku je količinu topline potrebno dovesti jediničnoj masi neke tvari
kako bi joj se temperatura povećala za jedinicu temperature
Mjerna jedinica za specifični toplinski kapacitet jest ili
Konačno, količina topline koju je potrebno dovesti tijelu mase
specifičnog toplinskog kapaciteta
kako bi mu se promijenila temperatura za
dana je formulom:
Tablica specifičnih toplinskih koeficijenata nekih tvari
| Tvar | c ( ) |
|---|---|
| alkohol | |
| aluminij | |
| bakar | |
| benzol | |
| cink | |
| led | |
| mesing | |
| olovo | |
| petrolej | |
| platina | |
| srebro | |
| staklo | |
| voda | |
| željezo |
Usporedite kojoj je od ovih dviju tvari potrebno dovesti više topline:
čeličnom loncu čija masa iznosi
i kojem želimo povećati temperaturu s
na
ili vodi volumena 1 L kojoj također želimo povećati temperaturu s
na
Pripremate li kupku ili vodu za pranje posuđa, iz iskustva vam je poznato da je potrebno pomiješati određenu masu vruće i hladne vode kako biste dobili smjesu odgovarajuće temperature.
Dio fizike
koji se bavi mjerenjem količine topline, određivanjem specifičnog toplinskog kapaciteta i učincima miješanja tvari različitih temperatura naziva se kalorimetrija.
Uređaj za mjerenje specifičnog toplinskog kapaciteta jest Richmannov kalorimetar.

Kalorimetar je dobro izolirana posuda čije su stijenke ispunjene toplinskim izolatorom koji sprječava toplinsko vođenje, odnosno izmjenu topline sadržaja kalorimetra s okolinom. Najčešći izolator u stijenkama kalorimetra jest zrak. U svakodnevnom životu često se koriste naprave slične kalorimetru, kao što su termos boca ili prijenosni hladnjak.
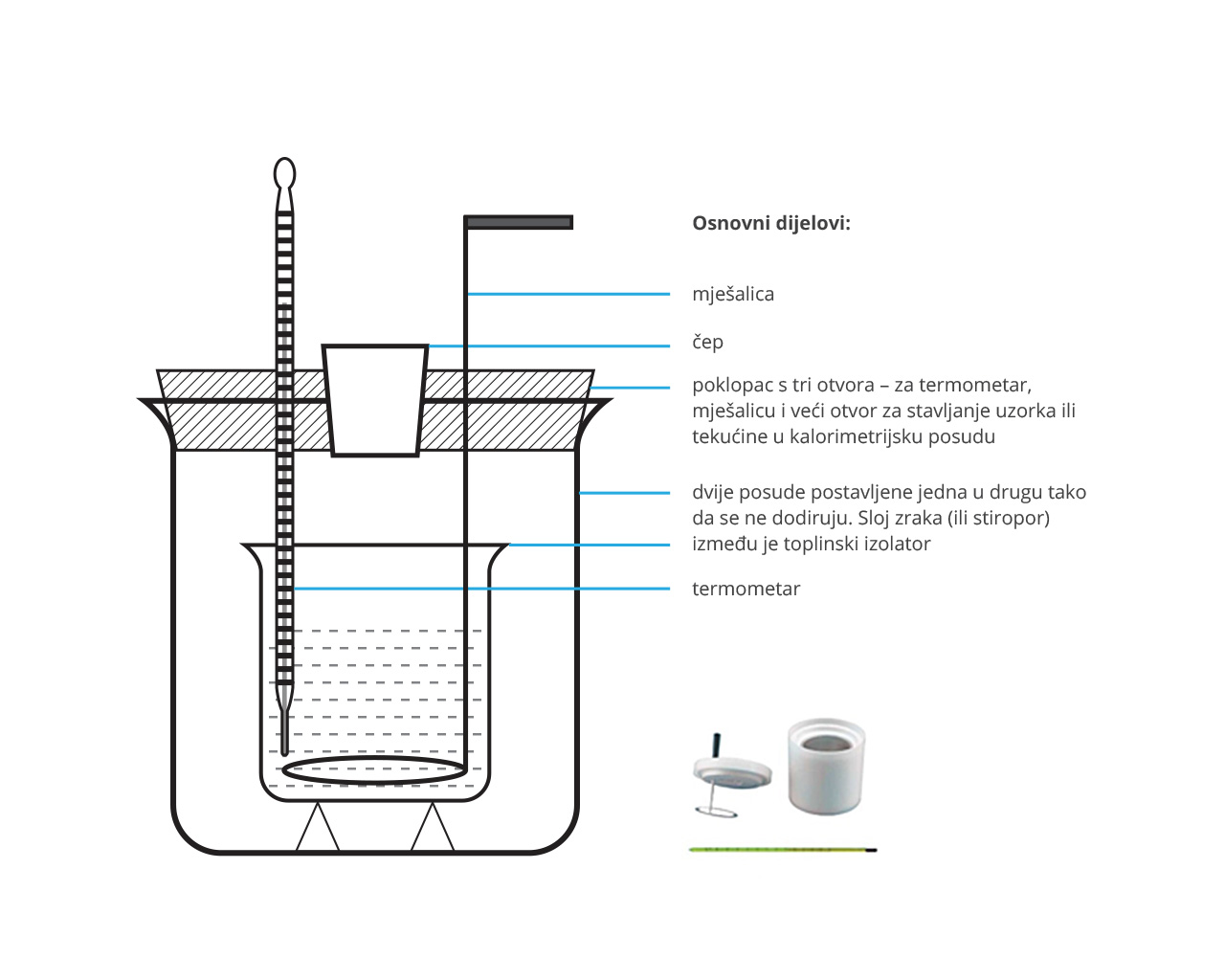
Kad se u tekućinu mase temperature koja se nalazi u kalorimetru, umiješa neka druga tekućina (ili se u nju uroni neka čvrsta tvar) mase i temperature dolazi do prijelaza topline s tvari više temperature na tvar niže temperature sve dok ne dođe do toplinske ravnoteže.
Zajednička temperatura naziva se temperatura smjese .
Zanemarimo li prijelaz topline u okolinu (gubitke), tada vrijedi Richmannovo pravilo ili metoda smjese.
Richmannovo pravilo kaže da je količina topline koju tijelo niže temperature primi od tijela više temperature jednaka količini topline koju tijelo više temperature preda tijelu niže temperature.
U formuli kojom je dano Richmannovo pravilo sljedeće su fizikalne veličine:
U lijevom dijelu jednakosti kojom je dano Richmanovo pravilo je promjena temperature tvari koja prima toplinu, a u desnom dijelu jednakosti je promjena temperature tvari koja predaje toplinu.
Ovakav zapis Richmannova pravila omogućava da su i lijeva i desna strana jednakosti pozitivnog predznaka.
U šalici se nalazi
vruće vode temperature
Koliko hladne vode temperature
treba dodati vrućoj da se dobije smjesa temperature
Pomoć:
Ovo je zadatak za čije riješavanje treba koristiti Richmannovo pravilo.
Postupak:
U prijenosnom hladnjaku nalazi se
posuda temperature
Masa svake posude iznosi
a toplinski kapacitet posuda iznosi
U prijenosni hladnjak naknadno su stavljene i dvije boce vode ukupne mase
koje su bile izvan hladnjaka. Toplinski kapacitet vode i boce zajedno iznosi
Prijelaz topline na sanduk zanemariv je. Kolika je temperatura boca s vodom prije nego što su stavljene u hladnjak, ako je konačna temperatura posuda i boca s vodom u hladnjaku
Temperatura boca s vodom prije stavljanja u hladnjak iznosi
Najvažniji pojmovi koje smo naučili u ovoj jedinici jesu unutarnja energija, toplina, toplinski kapacitet i Richmannovo pravilo.
Ukupan zbroj kinetičkih i potencijalnih energija molekula nekog čvrstog tijela, tekućine ili plina naziva se unutarnja energija .
Toplina je energija koja spontano prelazi s tijela koje ima višu temperaturu na tijelo koje ima nižu temperaturu dok im se temperature ne izjednače, odnosno dok se ne izjednače njihove unutarnje energije.
Toplinski kapacitet sposobnost je tijela da pohrani određenu količinu topline određena je njegovim toplinskim kapacitetom.
Richmannovo pravilo glasi: količina topline koju hladnije tijelo primi od toplijeg jednaka je količini topline koju toplije tijelo preda hladnijem.
Unutarnja energija jest mjera za zagrijanost nekog tijela.
Toplina je isto što i unutarnja energija.
Spojite odgovarajuće parove oznaka i mjernih jedinica za specifični toplinski kapacitet i toplinski kapacitet.
|
Mjerna jedinica za specifični toplinski kapacitet
|
|
|
Mjerna jedinica za toplinski kapacitet
|
|
|
Oznaka za specifični toplinski kapacitet
|
|
|
Oznaka za toplinski kapacitet
|
Energija koja sponatano prelazi s tijela više temperature na tijelo niže temperature naziva se , a energija koja je sadržana u tijelu zbog gibanja i međudjelovanja njegovih čestica
U jednadžbi
koja opisuje Richmannovo pravilo, veličina
predstavlja: .
Veličina
predstavlja .