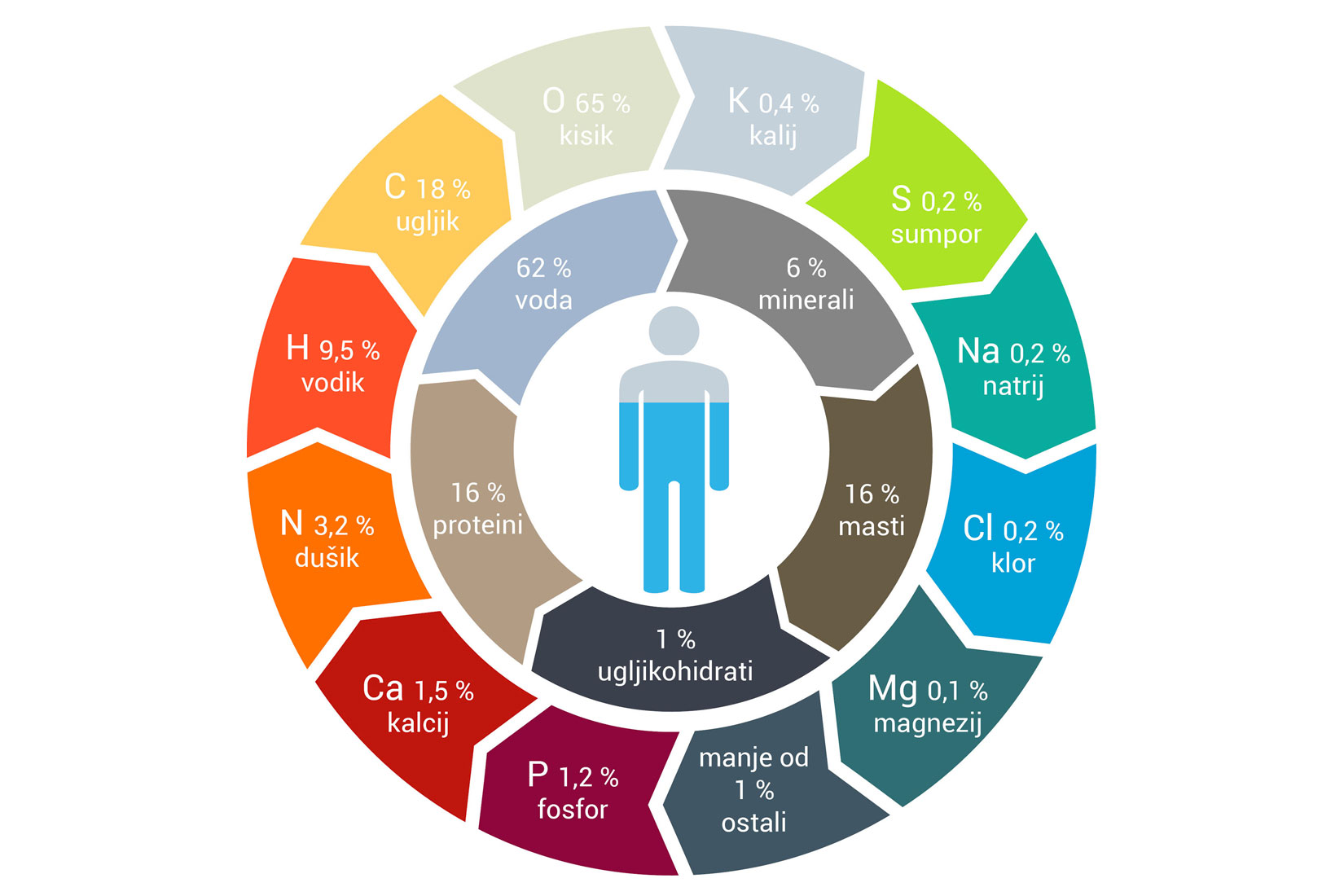
Tvari
1.1.Kemija i njezino značenje
Prve ljekarne u Europi



Neke otrovne biljke




1.2.Temeljni kemijski pojmovi i osnovna pravila pri izvođenju pokusa
Kako primijeniti znanstvenu metodu?

Posavjetujte se s nastavnikom kako ćete odrediti područje istraživanja, prikupljati literaturu, definirati ciljeve i istraživačka pitanja i oblikovati hipoteze.

Napravite nacrt istraživanja, odaberite uzorke za analizu i metode.

Obradite i analizirajte dobivene podatke. Prikažite rezultate istraživanja.
Kako primijeniti znanstvenu metodu?
Posavjetujte se s nastavnikom kako ćete odrediti područje istraživanja, prikupljati literaturu, definirati ciljeve i istraživačka pitanja i oblikovati hipoteze.
Napravite nacrt istraživanja, odaberite uzorke za analizu i metode.
Obradite i analizirajte dobivene podatke. Prikažite rezultate istraživanja.







Ormarić prve pomoći

- Uključite vagu pritiskom na tipku s oznakom POWER.

- Izvažite posudicu za vaganje ili papirnatu lađicu i zabilježite njihovu masu, .
- Uzorak kojem želite odrediti masu pažljivo stavite u posudicu za vaganje ili papirnatu lađicu za vaganje.
- Posudicu za vaganje ili papirnatu lađicu s uzorkom stavite na vagu i odčitajte masu, .

- Izračunajte masu uzorka i zabilježite ju u laboratorijski dnevnik, .
Kako nacrtati grafički prikaz podataka?

- Grafove valja crtati grafitnom olovkom na milimetarskom papiru kojeg treba zalijepiti u bilježnicu.
- Svaka se os (apscisa, os x, i ordinata, os y) označava oznakom vrste podataka i jedinicom u kojoj se mjeri. U ovom primjeru to su gustoća, iskazana u gramima po kubnom centimetru (ρ/gcm–3) i temperatura, iskazana u stupnjevima Celzijusa (t/°C).

- Odredi se veličina dijelova skale na osima.
- Ishodište koordinatnog sustava ne mora imati vrijednost nula, već vrijednost treba odabrati tako da se iskoristi veći dio površine milimetarskog papira.
- Veličina dijelova skale na osima ne mora biti jednaka.

- Podatke treba jasno naznačiti kao točke u grafu.

- Točke se povežu linijom. Dobivena krivulja ili pravac ne mora prolaziti kroz sve točke.
Definicije sedam osnovnih SI mjernih jedinica
METAR je duljina koju prevali svjetlost u vakuumu u dijelu sekunde.
SEKUNDA je trajanje 9 192 631 770 perioda zračenja koje nastaje elektronskim prijelazom između dviju hiperfinih energijskih razina atoma cezija u osnovnom stanju.
KELVIN je dio termodinamičke temperature trojne točke vode.
AMPER je jakost stalne istosmjerne struje koja teče kroz dva ravna, paralelna, beskonačno duga vodiča zanemariva presjeka razmaknuta 1 m u vakuumu, tako da stvara silu od N po metru dužine.
MOL je množina uzorka koji sadrži onoliko jedinki koliko atoma ima u 0,012 kg izotopa ugljika 12 C. Broj jedinki u molu je .
KANDELA je intenzitet zračenja što ga u okomitom smjeru emitira apsolutno crno tijelo površine pri temperaturi skrućivanja platine.
KILOGRAM je masa sadržana u međunarodnom prototipu utega (prautegu) koji se čuva u međunarodnom uredu za mjere i utege u Servesu kraj Pariza.
Definicije sedam osnovnih SI mjernih jedinica
METAR je duljina koju prevali svjetlost u vakuumu u dijelu sekunde.
SEKUNDA je trajanje 9 192 631 770 perioda zračenja koje nastaje elektronskim prijelazom između dviju hiperfinih energijskih razina atoma cezija u osnovnom stanju.
KELVIN je dio termodinamičke temperature trojne točke vode.
AMPER je jakost stalne istosmjerne struje koja teče kroz dva ravna, paralelna, beskonačno duga vodiča zanemariva presjeka razmaknuta 1 m u vakuumu, tako da stvara silu od N po metru dužine.
MOL je množina uzorka koji sadrži onoliko jedinki koliko atoma ima u 0,012 kg izotopa ugljika 12 C. Broj jedinki u molu je .
KANDELA je intenzitet zračenja što ga u okomitom smjeru emitira apsolutno crno tijelo površine pri temperaturi skrućivanja platine.
KILOGRAM je masa sadržana u međunarodnom prototipu utega (prautegu) koji se čuva u međunarodnom uredu za mjere i utege u Servesu kraj Pariza.
1.3.Izvori tvari
Dobivanje soli u solani u Stonu




1.4.Fizikalna i kemijska svojstva tvari
1.5.Podjela tvari i postupci odjeljivanja tvari

Isparavanje
Isparavanje je jedan od postupaka razdvajanja smjese sastavljene od tvari različitog vrelišta, odnosno različite hlapljivosti. Isparavanjem otapala iz otopina čvrstih tvari izdvaja se čvrsta tvar.

Sedimentacija
Sedimentacija (taloženje, slijeganje na dno) je postupak odjeljivanja specifično teže (gušće) suspendirane tvari od otopine. Čvrsta tvar se slegne na dno, a tekućina se iznad nje odlije (dekantira).


Odjeljivanje pomoću magneta
Željezo, kobalt, nikal i njihove legure su magnetični pa se to svojstvo koristi za njihovo izdvajanje iz heterogene smjese tvari.
Kristalizacija
Kristalizacija je postupak izlučivanja kristala iz zasićene otopine. Otopina koja pri određenom tlaku i temperaturi ne može otopiti novu količinu tvari naziva se zasićenom otopinom. Topljivost većine soli u vodi raste s povišenjem temperature. Hlađenjem zasićenih otopina tog tipa otopljena se tvar izlučuje u obliku kristala jer se pri nižoj temperaturi u istoj količini otapala može otopiti manje tvari.
Kristalizacijom čvrste tvari u otopini ostaju nečistoće pa su izlučeni kristali čišći od uzorka tvari prije otapanja. Postupak kristalizacije prethodno otopljenih kristala naziva se prekristalizacijom.

Sublimacija
Sublimacija je postupak odjeljivanja tvari iz smjese, pri čemu jedan sastojak prelazi iz čvrstog u plinovito agregacijsko stanje. Tvari koje sublimiraju su jod, naftalen, kamfor i dr.
Kristalizacija
Kristalizacija je postupak izlučivanja kristala iz zasićene otopine. Otopina koja pri određenom tlaku i temperaturi ne može otopiti novu količinu tvari naziva se zasićenom otopinom. Topljivost većine soli u vodi raste s povišenjem temperature. Hlađenjem zasićenih otopina tog tipa otopljena se tvar izlučuje u obliku kristala jer se pri nižoj temperaturi u istoj količini otapala može otopiti manje tvari.
Kristalizacijom čvrste tvari u otopini ostaju nečistoće pa su izlučeni kristali čišći od uzorka tvari prije otapanja. Postupak kristalizacije prethodno otopljenih kristala naziva se prekristalizacijom.