Nezasićeni ugljikovodici – alkini
- povezati pojam nezasićenosti s prisutnošću trostruke veze između ugljikovih atoma u molekuli alkina
- objasniti svojstva, upotrebu i način dobivanja etina.
Uvod
Autogeno zavarivanje jest spajanje metalnih dijelova užarenih s pomoću plamena visoke temperature.
Rezanje metala jest odvajanje metalnih dijelova užarenih s pomoću plamena isto tako visoke temperature.
Tako visoka temperatura postiže se izgaranjem smjese kisika i plina etina te ima vrlo veliku primjenu u industriji.
Etin (stari naziv: acetilen) najjednostavniji je nezasićeni ugljikovodik s trostrukom vezom između dvaju atoma ugljika.
Uvod
Autogeno zavarivanje i rezanje metala jest spajanje i odvajanje metalnih dijelova užarenih s pomoću plamena visoke temperature. Temperatura izgaranja etina može doseći i 3100 °C. Za zavarivanje se acetilen rabi kao gorivi plin, a kisik kao plin koji podržava gorenje.
Etin, poznatiji po starom nazivu – acetilen, najjednostavniji je nezasićeni ugljikovodik s trostrukom vezom između dvaju atoma ugljika.
Nezasićeni ugljikovodici – alkini
Ugljikovodici s jednom ili više trostrukih veza između ugljikovih atoma pripadaju nezasićenim spojevima – alkinima. Prvi član u homolognom nizu alkina ima dva ugljikova atoma u svojemu sastavu. Opća molekulska formula alkina s jednom trostrukom vezom jest:
pri čemu je n broj ugljikovih atoma u molekuli. U imenovanju alkina koristi se nastavak: -IN.
Ako se u molekuli ugljikovodika nalaze i dvostruka i trostruka veza, dvostruka veza ima prednost u imenovanju, ali je trostruka veza reaktivniji dio molekule.
Homologni niz alkina s jednom trostrukom vezom u molekuli naveden je u tablici 1.
| redni broj u homolognom nizu |
ime ugljikovodika | molekulska formula |
|---|---|---|
| 1. | ETIN | |
| 2. | PROPIN | |
| 3. | BUTIN | |
| 4. | PENTIN | |
| 5. | HEKSIN | |
| 6. | HEPTIN | |
| 7. | OKTIN | |
| 8. | NONIN | |
| 9. | DEKIN |
Molekule alkina prikazujemo molekulskom, strukturnom i sažetom strukturnom formulom. Pogledajte na primjeru molekule etina.
Nije moguća rotacija atoma ugljika oko trostruke veze. Strukturni izomeri alkina mogući su samo u slučaju drugačijeg razmještaja ugljikovih atoma u molekuli i u slučaju drugačije pozicije trostruke veze u molekuli.
| ime spoja | pent-1-in | pent-2-in | 3-metilbut-1-in |
|---|---|---|---|
| molekulska formula | |||
| model sastavljen od kuglica i štapića | 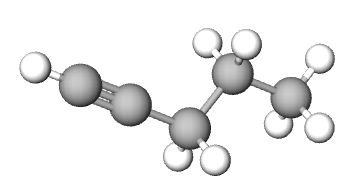 |
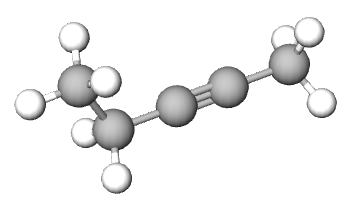 |
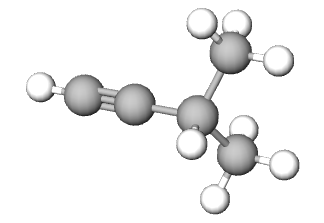 |
Osim lančanih alkina, također postoje i prstenasti ugljikovodici s trostrukom vezom.
Karakteristične kemijske reakcije alkina također su gorenje i adicija, kao i za alkene.
Etin – svojstva, dobivanje i upotreba
Svojstva etina:
• plin bez boje, karakteristična mirisa
• ima manju gustoću od zraka
• reaktivan je, zapaljiv, gori svijetlim i čađavim plamenom
• u vodi je slabo topljiv, dok je izvrsno topljiv u acetonu
• pod povišenim je tlakom eksplozivan.
Dobivanje etina:
I u industriji i u laboratoriju, temeljni proces dobivanja etina jest reakcija kalcijeva karbida i vode:
.
Kao i za alkene, karakteristične kemijske reakcije alkina također su gorenje i adicija.
Gorenje etina uz dovoljnu količinu kisika možemo prikazati sljedećom jednadžbom kemijske reakcije:
.
Nezasićenost alkina možemo ispitati reagensima: bromnom vodom i vodenom otopinom kalijeva permanganata. Kao što je opisano kod alkena, i alkini će obezbojiti reagense. Gubitak boje reakcijske smjese pozitivna je reakcija na nezasićenost.
U reakcijama adicije alkini će trošiti dvostruko više halogena od alkena jer se tijekom adicije alkin prevodi u alkan. Jednadžbe kemijske reakcije adicije obično se pišu sažetom strukturnom formulom radi preglednosti. Prikazana je jednadžba adijcije broma na etin pri čemu nastaje 1,1,2,2-tetrabrometan.
Etin – svojstva, dobivanje i upotreba
Svojstva etina
Etin je plin bez boje, karakteristična mirisa, manju gust od zraka. Reaktivan je, zapaljiv, gori svijetlim i čađavim plamenom. U vodi je slabo topljiv, dok je izvrsno topljiv u acetonu. Pod povišenim je tlakom eksplozivan pa se skladišti i prevozi u čeličnim bocama, otopljen u acetonu.
Dobivanje etina
I u industriji i u laboratoriju, temeljni proces dobivanja etina jest reakcija vode i kalcijeva karbida:
.
Pogledajte sljedeći videozapis i zaključite razvija li se u pokusu plin etin.
Upotreba etina
Zbog svijetlog plamena pri gorenju etin je korišten za izradu rudarskih karbidnih svjetiljki, a i danas se troši u većim količinama za rad svjetionika. Etin je osnovna sirovina za proizvodnju brojnih drugih organskih spojeva (npr. boje, lijekovi, plastične mase).
Na kraju…
Karbidna svjetiljka – suputnik rudarima, geolozima i speleolozima
Kalcijev karbid, , prvi je put proizveden 1892. godine, a karbidne lampe u rudarstvu korištene su već 1913. godine u rudniku žive u Idriji. Najstariji podatak o upotrebi karbidne lampe u Hrvatskoj potječe iz 1935. godine kada je zabilježena da se koristila pri istraživanju špilja Velike Paklenice (geolog Josip Poljak).
Više o povijesti korištenja karbidnih svjetiljki saznajte iz izdanja Hrvatskog planinarskog saveza: “Razvoj rasvjete za speleološke potrebe” (Vlado Božić).
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan ili više točnih odgovora.
Odaberite sve točne odgovore.
Odaberite svojstva etina (tri su odgovora točna).
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Nezasićenost alkina možemo ispitati reagensima: bromnom vodom i vodenom otopinom kalijeva permanganata. Gubitak boje reagensa pozitivna je reakcija na nezasićenost.
Želite li pokušati ponovo?
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Kako glasi molekulska formula za heks-2-in?
Povlačenjem elemenata uskladi odgovarajuće parove.
Spojite parove premještajući pojmove po stupcima.
Pojmovima u lijevom stupcu pridružite odgovarajući pojam u desnom stupcu.
adicija
acetilen
etin
reakcija pripajanja na nezasićenu vezu
kalcijev karbid i voda
reaktanti čijom reakcijom dobivamo etin
produkti gorenja etina uz dovoljnu količinu kisika
ugljikov dioksid i voda
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Kako se zove spoj čija je strukturna formula
?
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Adicijom klorovodika na propin dobije se:
Želite li pokušati ponovo?