Sapuni i deterdženti
- objasniti proces saponifikacije
- protumačiti mehanizam pranja
- protumačiti svrsishodno korištenje sredstava za pranje u kućanstvu prema vrsti nečistoće
- vrednovati prednosti i nedostatke sapuna i deterdženata
- razvijati interes za sastav kemikalija u općoj upotrebi, kućanstvu i kozmetici.
Uvod
Sapunika, Saponaria officinalis, L., zeljasta je biljka iz porodice karanfila. Raste na vlažnim i sjenovitim mjestima, uz šume, potoke i rijeke. Uz ljekovita svojstva, sapunika se koristi na još jedan zanimljiv način. Njezin podanak (podzemna stabljika) korišten je za pranje tijela i odjeće već u doba praljudi.
Sapunika ima razgranat i deblji podanak izvana crvenosmeđe boje, a iznutra žute boje. Podanak sapunike sadrži mnogo saponina. Ako se podanak usitni i gnječi u vodi, stvara se bogata pjena pogodna za pranje.
Zanima li vas što su saponini? Pokušajte u suradnji s prijateljima iz razreda istražiti tu vrlo zanimljivu skupinu tvari!
Sapuni
Sapune dobivamo procesom saponifikacije.
To je reakcija lužnate razgradnje estera (biljne i životinjske masti).
Pri tome nastaju alkohol glicerol i sapuni (soli masnih kiselina).
Sljedeća slika prikazuje opću jednadžbu procesa saponifikacije.
Sapuni
Sapuni su po kemijskom sastavu natrijeve ili kalijeve soli viših masnih kiselina. Sapune dobivamo procesom saponifikacije. To je reakcija lužnate razgradnje estera (biljne i životinjske masti), a produkti su te reakcije alkohol glicerol i sapuni (soli masnih kiselina). Sljedeća slika prikazuje opću jednadžbu procesa saponifikacije.
Kod kuće najčešće koristimo natrijeve, tvrde sapune u čijemu se sastavu nalaze brojne tvari za njegu kože.
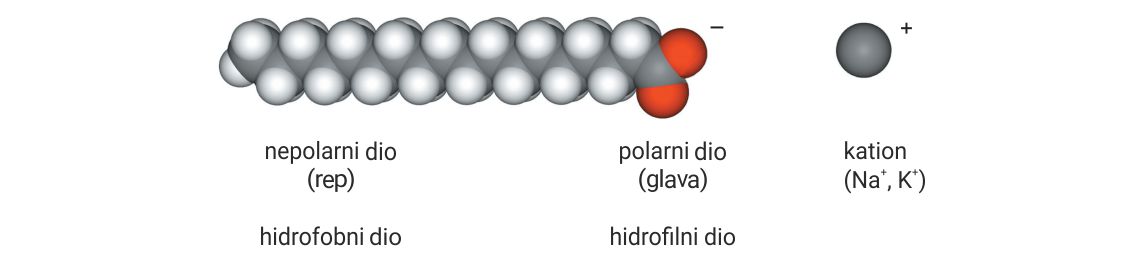
Najvažniji sastojak proizvoda ipak je tvar koja obavlja pranje, a to je molekula sapuna, najčešće natrijev stearat.
Kako sapun djeluje na nečistoće?
Premda je molekula sapuna amfipatska i njezin je veći dio nepolaran, sapun se vrlo dobro otapa u vodi.
Najčešće nečistoće na tkaninama jesu masnoće.
Pri pranju će molekule sapuna svojim nepolarnim krajem ući u česticu masnoće.
Trljanjem tkanine od nje će se odvojiti manji broj molekula sapuna, zajedno s dijelom nečistoće, te će prijeći u vodu.
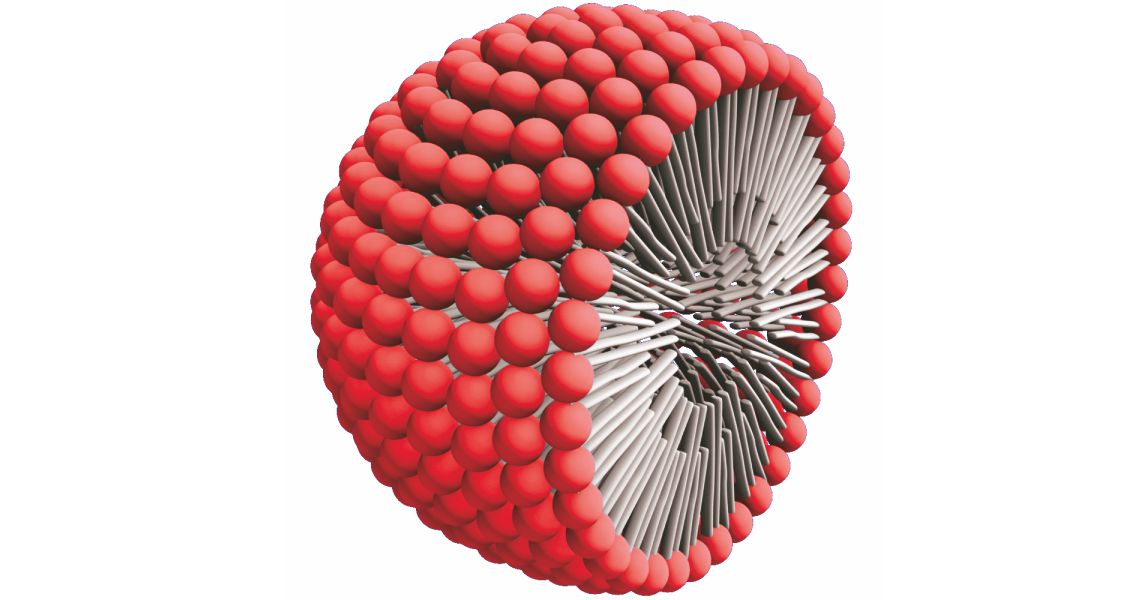
U vodi će se od njih stvoriti kuglasta struktura koju nazivamo micela.
Pri tome se najprije događa disocijacija molekule sapuna na ione. Prikažimo taj proces na primjeru natrijeva stearata:
.
Stearatni anioni, , u vodi se međusobno orijentiraju tako da se hidrofobni dijelovi molekule (ugljikovodični lanci) okrenu jedan prema drugome. Prema vodi su tako okrenuti hidrofilni dijelovi molekule (polarna karboksilna skupina). Tako nastali dvosloj molekula sapuna veže na sebe molekule vode.
Dio molekula sapuna raspoređuje se na površini vode tako da je hidrofilni dio molekule okrenut u vodu, a hidrofobni dio prema zraku. Tako molekule sapuna smanjuju pojavu površinske napetosti vode.
Masnoće su najčešće nečistoće na tkaninama. Pri pranju molekule sapuna svojim će hidrofobnim krajem ući u česticu masnoće. Trljanjem tkanine od nje će se odvojiti manji broj molekula sapuna s dijelom nečistoće te će prijeći u vodu. U vodi će se od njih stvoriti kuglasta struktura koju nazivamo micela.
U unutrašnjosti micele nalazi se manji dio nečistoće, a na površini micele nalaze se polarne skupine molekula sapuna koje privlače vodu.
Na kraju pranja ispiremo tkaninu čistom vodom. Pri tome voda odnosi nastale micele i višak sapuna.
U unutrašnjosti micele nalazi se manji dio nečistoće, a na površini micele nalaze se polarne, hidrofilne skupine molekula sapuna koje privlače vodu. Na kraju pranja ispiremo tkaninu čistom vodom. Pri tome voda odnosi nastale micele i višak sapuna.
Sapuni su bolje topljivi u mekoj vodi poput kišnice, deionizirane i destilirane vode. Zato su nekoć domaćice radije skupljale kišnicu nego sapunom prale rublje na potoku. U tvrdoj vodi potoka veća je količina kalcijevih iona zbog kojih se sapun taloži. Kod pranja u tvrdoj vodi jedan će se dio sapuna utrošiti na taloženje s kalcijem, a tek preostali dio koristit će se za pranje.
Važnost održavanja higijene ruku
Održavanje higijene tijela, odjeće i prostora preduvjet je očuvanja zdravlja. Svakodnevno pranje ruku sapunom nužno je za vlastito zdravlje, a osobito je važno u medicini. Liječnici kirurzi na poseban način temeljito peru ruke prije obavljanja operacija.
Izrada sapuna u domaćinstvu
Proizvodnja sapuna odavno je poznata. Povijest bilježi zapise o izradi sapuna u drevnom Babilonu, Egiptu, Sumeru i Rimu. Sapun su poznavali Kelti, Gali i Arapi. U 8. stoljeću sapun se već proizvodi u Veneciji, Genovi i južnoj Francuskoj.
Zanimljivo je istaknuti da se na početku sapun koristio bez vode i u medicinske svrhe. Industrijska proizvodnja sapuna počinje u 18. stoljeću, a tek poslije Prvog svjetskog rata postaje roba široke potrošnje. Brojni mediteranski gradovi imaju vlastite, sebi svojstvene, recepte za sapun.
Unatoč vrlo razvijenoj industriji, ljudi su zadržali tradiciju izrade sapuna u kućnoj radionosti. U industrijskim sapunima neki sastojci mogu izazvati alergijske reakcije na koži ili druge neželjene pojave. Zato se sve veći broj ljudi vraća proizvodnji i korištenju domaćih sapuna.
Tijekom proizvodnje sapuna često se osnovnoj smjesi dodaje razno ljekovito bilje i prirodna biljna ulja.

Recept za kuhanje sapuna iz Praktične kuharice (1923. godina)
Prvi recept: Na 1 kg otpadne masti (na primjer čvarci, loj, salo itd.) uzmite 2 litre kišnice, kg sode, kg vapna. Vapno razmutite u vodi, procijedite kroz gusto sito ili krpu i pustite da prokuha. Zatim ga malo rashladite vodom i dodajte sodu (poklopite da se ne rashladi). Opet stavite da samo malo prokuha pa dodajte otpatke. Sapun treba miješati, a kuha se po prilici 2 – 3 sata. (Uzmite malo sapuna u žlicu. Ako se stvrdne, gotov je.) Kad bude skoro gotov, priredite korito i unutra stavite mokru krpu. Kad sapun bude gotov, istresite ga u korito da se stvrdne, a onda izrežite u komade. Izrezani sapun stavite na suho mjesto na zraku da se suši.
Drugi recept: 9 l kišnice, 3 kg loja, 1 kg ljute sode (lužni kamen, njem. der Laugenstein). Sve pristavite i pomalo dolijevajte vodu uz neprestano miješanje. Kuhajte oko 1 sat da postane gusto, zatim dodajte 1 šaku soli i malo prokuhajte. Odmah skinite s vatre i istresite u sanduk.
Deterdženti
Deterdženti su sredstva za pranje koja se većinom proizvode od naftnih prerađevina. Po kemijskom sastavu deterdženti su slični sapunima i također imaju amfipatske molekule. Ugljikovodični, hidrofobni, dio molekule deterdženta može biti ravan ili razgranat. Hidrofilni dio molekule deterdženta, za razliku od sapuna, sadrži sulfatnu, OSO3 –, odnosno sulfonatnu, SO3 –, skupinu pa opća formula deterdženta može biti npr. , odnosno .
Za razliku od sapuna, deterdženti mogu prati u tvrdoj i u blago kiselim vodama. Mehanizam pranja deterdžentima isti je kao i kod sapuna. Sapune i deterdžente nazivamo još i površinski aktivne tvari jer smanjuju pojavu površinske napetosti vode.
Deterdženti u kućanstvu najčešće se koriste za strojno i ručno pranje rublja i posuđa. Razlikuju se po sastavu i količini aktivnih tvari. Deterdženti za pranje rublja sadrže samo manji dio aktivnih molekula za pranje (oko 15 %), ostalo su sredstva za omekšavanje vode, lužnate soli, enzimi, optička bjelila, stabilizatori, mirisi, sredstva za izbjeljivanje i drugo. Obično su sredstva za strojno pranje jako lužnata i nisu pogodna za ručno pranje.
Etiketa na ambalaži proizvoda za pranje
Suvremena sredstva za pranje svojim su sastavom prilagođena za određenu namjenu. To je poznato svima koji su barem jednom pokušali oprati kosu sapunom umjesto šamponom. Zato je važno čitati etikete proizvoda i upoznati sastav i namjenu proizvoda prije nego što se odlučimo na kupnju.
Uz klasične kemijske piktograme, na etiketi i ambalaži proizvoda nalaze se razni znakovi i slike.
Istražite i saznajte što znače oznaka “CE”, slika zeca, crna i bijela strelica zajedno u krugu, otvorena kutijica i drugo.
Na etiketi bočice tekućeg sapuna pročitajte sastav. Što je zapravo po kemijskom sastavu “tekući sapun”?
Utjecaj sredstava za pranje na okoliš
Opažen je negativan utjecaj otpadnih voda s deterdžentima na prirodne vodene ekosustave. Biološka razgradivost prvih proizvedenih deterdženata bila je manja nego što je to danas. Uzrok tome jest razlika u strukturi molekule deterdženata. Prvotni su deterdženti imali molekule s razgranatim ugljikovodičnim lancima, a takve molekule bakterije u prirodnim vodama nisu mogle razgraditi.
Mikroorganizmi mogu biološki razgraditi samo ravnolančane ugljikovodične dijelove molekule. S pomoću svojih enzima mikroorganizmi odcjepljuju dva po dva ugljika iz molekule deterdženta. Ako molekula deterdženta ima razgranat ugljikovodični lanac, mikroorganizmi neće moći razgraditi takvu molekulu. Stoga se u sastavu deterdženta treba nalaziti što više molekula deterdženta s ravnolančanim molekulama.
Također je utvrđen negativan učinak povećane količine fosfata koji u sastavu deterdženata služe za omekšavanje vode. Veća količina fosfata uzrok je pojave cvjetanja mora, tj. naglog razmnožavanja planktonskih algi. Fosfati nisu štetni u manjoj količini, ali u povećanoj količini uzrokuju pretjeran rast algi zbog čega prirodne vode postaju mutne. U konačnici to smanjuje količinu svjetlosti u vodi i tako izravno utječe na smanjenje fotosinteze. U ekosustavu se proizvodi manje hrane, a to utječe na brojnost populacija.
U prirodnim vodama mikroorganizmi mogu vrlo lako razgraditi molekule sapuna i deterdženata koji imaju ravne ugljikovodične dijelove molekule. Zato suvremeni deterdženti ne sadrže fosfate, a aktivne su tvari većim dijelom ravnolančane molekule deterdženata.