Aromatski ugljikovodici
- objasniti svojstva, upotrebu i način dobivanja benzena
- razviti vještinu crtanja strukturne formule benzena
- objasniti postojanost benzenskog prstena
- objasniti kemijske reakcije benzena
- razlikovati aromatične spojeve od spojeva aromatskog karaktera.
Uvod
Što je TNT?
Ljubitelji i dobri poznavatelji stripa pojam TNT povezuju sa simpatičnom ekipom Alana Forda, ali što je TNT u kemijskom svijetu? Imaju li Fordova ekipa i TNT ipak nešto zajedničko?
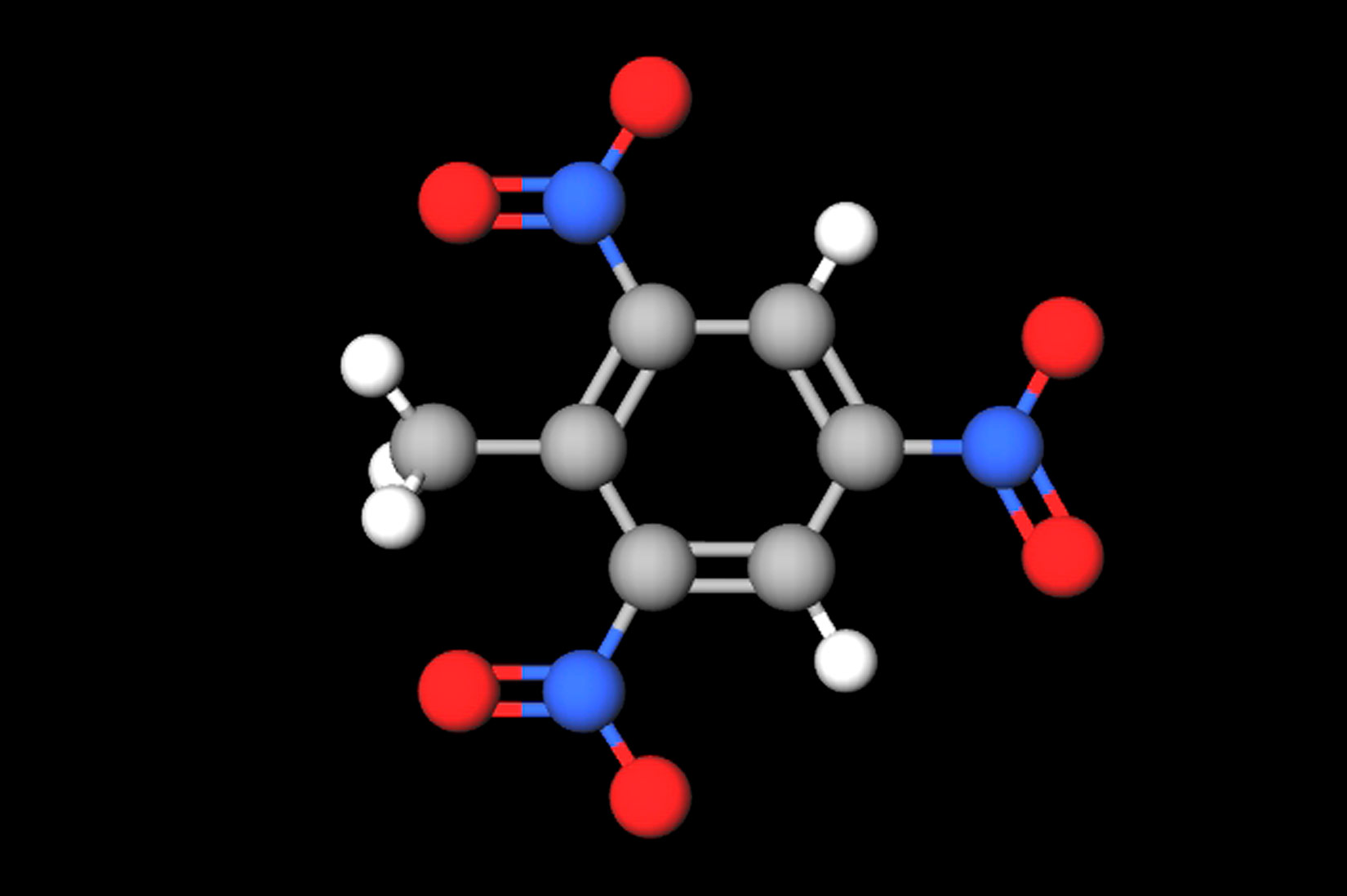
Puni naziv kemijskog spoja čija je kratica TNT glasi: trinitrotoluen. Za mjerenje količine energije koja se oslobađa eksplozijom koristi se mjerna jedinica TNT ekvivalent, što odgovara energiji oslobođenoj eksplozijom jedne tone TNT-a.
Aromatski ugljikovodici – areni
Aromatski ugljikovodici ili ARENI čine posebnu skupinu prstenastih ugljikovodika jer imaju karakterističnu građu i svojstva.
Prvi aromatski ugljikovodici izolirani su iz aromatičnih smola pa su dobili ime po grčkoj riječi aroma (mirisna trava).
Ako organski spoj sadrži barem jedan prsten od šest ugljikovih atoma, kažemo da ima svojstvo aromatičnosti.
Pri tome svi ugljikovi atomi u prstenu leže u istoj ravnini, sve veze između ugljikovih atoma jednake su duljine i vezni kutovi iznose 120°.
Puni naziv kemijskog spoja čija je kratica TNT glasi: trinitrotoluen. Za mjerenje količine energije koja se oslobađa eksplozijom koristi se mjerna jedinica TNT ekvivalent, što odgovara energiji oslobođenoj eksplozijom jedne tone TNT-a.
Aromatski ugljikovodici – areni
Aromatski ugljikovodici ili ARENI čine posebnu skupinu prstenastih ugljikovodika jer imaju karakterističnu građu i svojstva. Prvi aromatski ugljikovodici izolirani su iz aromatičnih smola pa su po tome dobili ime (grč. aroma – mirisna trava).
Danas se pod svojstvom aromatičnosti podrazumijeva da organski spoj sadrži barem jedan prsten od šest ugljikovih atoma. Pri tome svi ugljikovi atomi u prstenu leže u istoj ravnini, sve veze između ugljikovih atoma jednake su duljine i vezni kutovi iznose 120°. Od svakog ugljikova atoma u aromatskom prstenu po jedan je elektron delokaliziran. To znači da taj elektron ne pripada točno nekom atomu ugljika, već je sastavni dio elektronskog oblaka koji se proteže preko čitava aromatskog prstena. Takvo svojstvo aromatskog prstena daje posebnu stabilnost i označava aromatičnost.
Najjednostavniji aromatski spoj jest benzen koji u svojoj građi ima jedan aromatski prsten.
Areni složenije strukture imaju dva, tri i više aromatskih prstena.
Pokušajte, služeći se programom ChemSketch za crtanje kemijskih spojeva s pomoću računala, načiniti prikaze strukturnih formula za sljedeće aromatske spojeve: benzen, , naftalen, , i antracen, .
Načinjene prikaze strukturnih formula postavite na Padlet i svoje uratke međusobno usporedite i prokomentirajte s učiteljicom/učiteljem na satu.
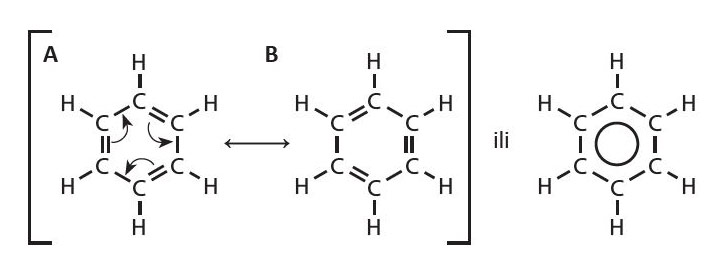
Struktura molekule benzena,
U strukturnoj formuli molekule benzena, unutar šesterokuta, između atoma ugljika prikazujemo naizmjenično jednostruke i dvostruke veze. Budući da se jednostruka i dvostruka veza razlikuju u duljini i energiji, bolji je način prikazivanja šesterokut s upisanom kružnicom. Naime, ustanovljeno je da su udaljenosti između ugljikovih atoma zapravo jednake i po duljini i po energiji.
Kod takva prikaza molekule benzena prikazan je samo benzenski aromatski prsten, dok se simboli ugljika i vodika te veze ugljika i vodika ne prikazuju.
Svojstva benzena
Benzen je bezbojna tekućina, svojstvenoga mirisa i lako je zapaljiva. Smjesa benzenskih para i zraka eksplozivna je. Benzen je otrovan i kancerogen. Prvi je put izoliran iz katrana kamena ugljena 1825. g.
U kemijskoj industriji benzen je otapalo za masti, ulja, smole i boje, a također je važan kao sirovina za proizvodnju mnogih kemijskih spojeva. Zbog njegova štetna djelovanja, umjesto benzena, koriste se njegovi derivati koji nisu toliko štetni.
Kemijske reakcije benzena
Benzen pripada u nezasićene ugljikovodike, međutim ipak radije ostvaruje kemijske reakcije supstitucije – zamjene svojih vodikovih atoma.
Najvažnije kemijske reakcije benzena obuhvaćaju reakcije s halogenim elementima, dušičnom kiselinom i sumpornom kiselinom.
Produkti tih reakcija su važni proizvodi poput detergenata, pesticida, eksploziva, lijekova i plastičnih masa.
Areni – kancerogene tvari
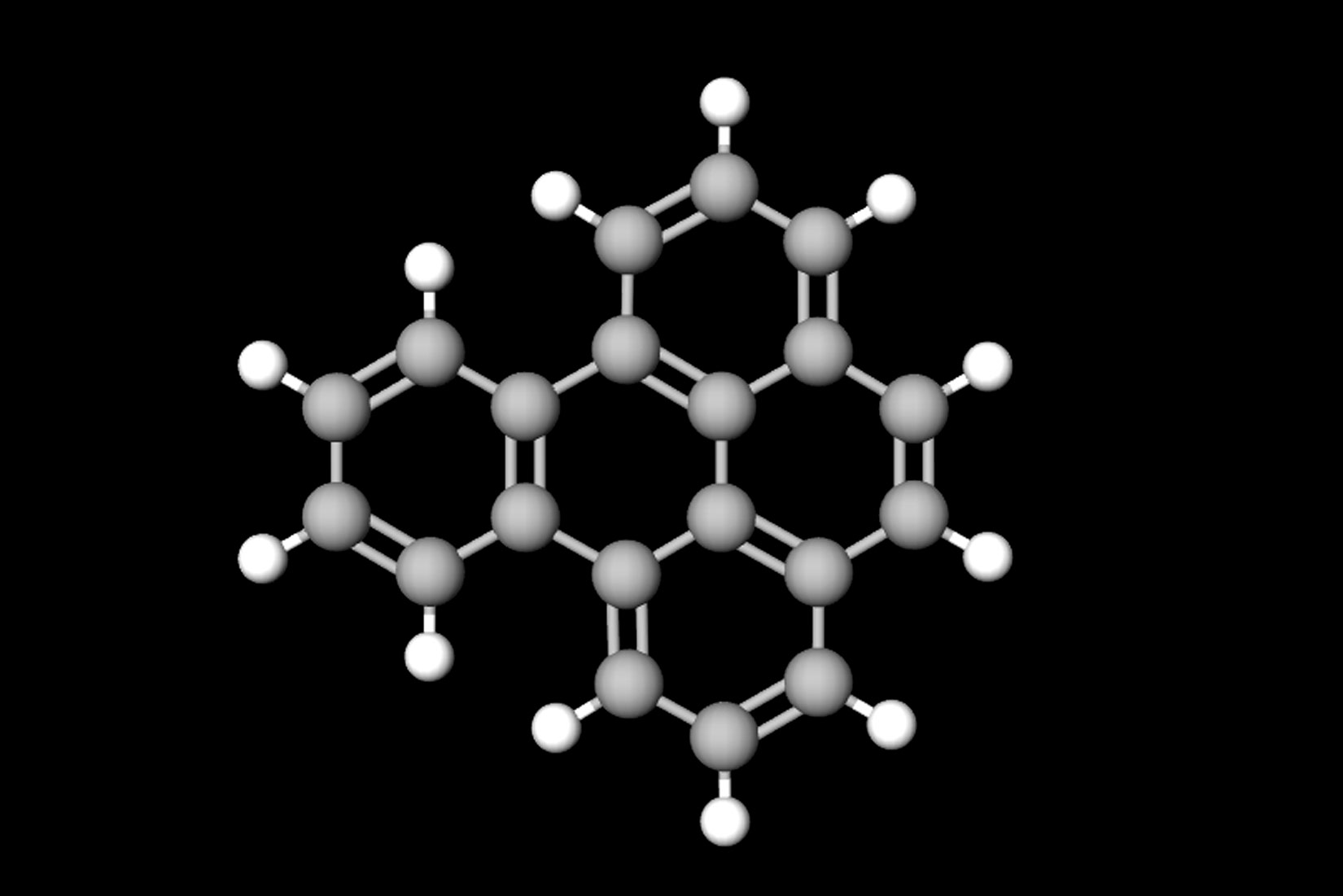
Benzopiren se prirodno stvara gorenjem drveta, benzina i fosilnih goriva. Nastaje i pri vulkanskim erupcijama, u duhanskom dimu i prženoj hrani. Nepovoljno utječe na zdravlje, povezuje se sa tumorom pluća. Prije 200 godina u Engleskoj je zabilježen velik broj oboljelih dimnjačara od raka pluća.
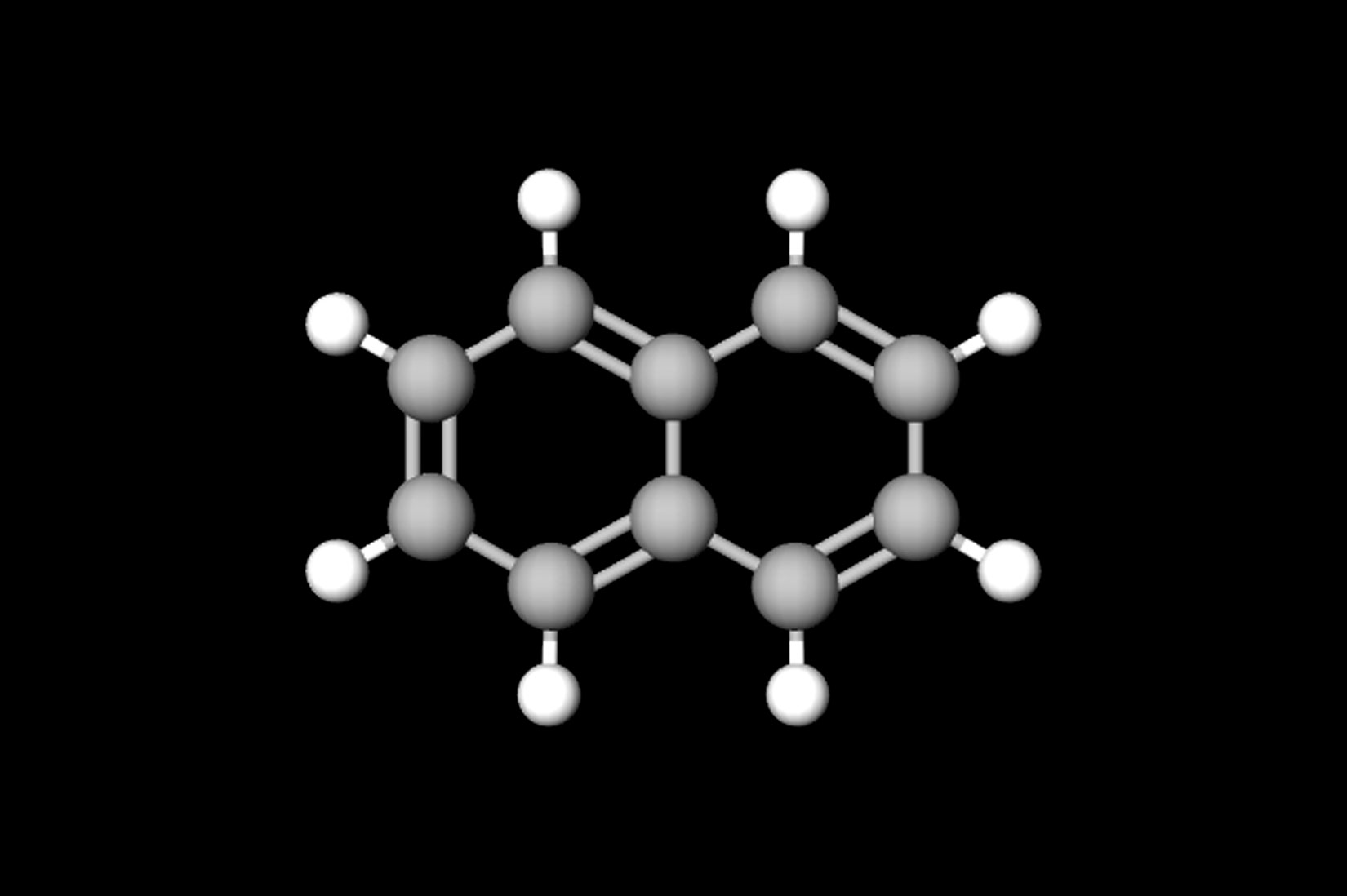
Naftalen je bijela čvrsta tvar u obliku sjajnih kristalića, lako sublimira i masnog je opipa. Zapaljiv je i gori svijetlim i čađavim plamenom. Također je kancerogena tvar pa je napušteno njegovo korištenje. U prošlosti se koristio u velikim količinama kao insekticid, kao sredstvo za konzerviranje drva i kao štavilo za kožu.
Kemijske reakcije benzena
Benzen pripada nezasićenim ugljikovodicima, ali je za njega karakteristična kemijska reakcija supstitucije, tj. zamjene vodikovih atoma. To se događa zbog stabilne aromatske jezgre benzena čije je narušavanje energijski nepovoljno, stoga se teško događa. Zato benzen pokazuje negativnu reakciju na testne reagense koji ispituju nezasićnost organskih spojeva.
Najvažnije kemijske reakcije
Areni – kancerogene tvari
Benzopiren se prirodno stvara gorenjem drveta, benzina i fosilnih goriva. Nastaje i pri vulkanskim erupcijama, u duhanskom dimu i prženoj hrani. Nepovoljno utječe na zdravlje i povezuje se s tumorom pluća. Prije 200 godina u Engleskoj je zabilježen velik broj dimnjačara oboljelih od raka pluća.
Naftalen je bijela čvrsta tvar u obliku sjajnih kristalića, lako sublimira i mastan na opip. Zapaljiv je i gori svijetlim i čađavim plamenom. Također je kancerogena tvar pa se više ne koristi. U prošlosti se koristio u velikim količinama kao insekticid, kao sredstvo za konzerviranje drva i kao štavilo za kožu.
Areni – korisne tvari
Nisu svi aromatski spojevi štetni. Upoznajte i neke korisne arene koji su važni lijekovi ili antioksidans.
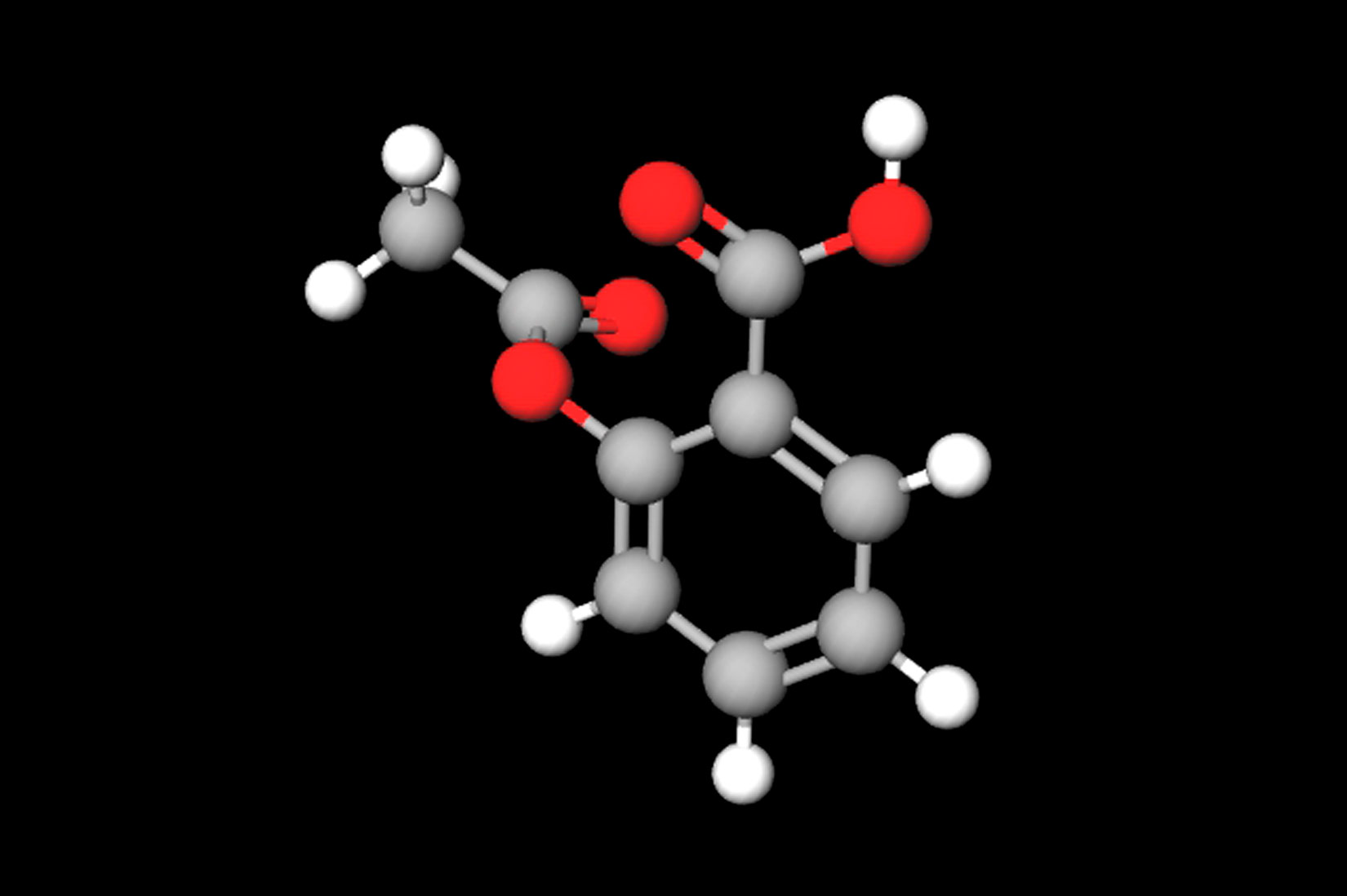
- Aspirin je najpoznatiji lijek protiv bolova, upale i temperature. Koristi se i za poboljšanje funkcije krvotoka i srca i sprečava stvaranje krvnih ugrušaka.
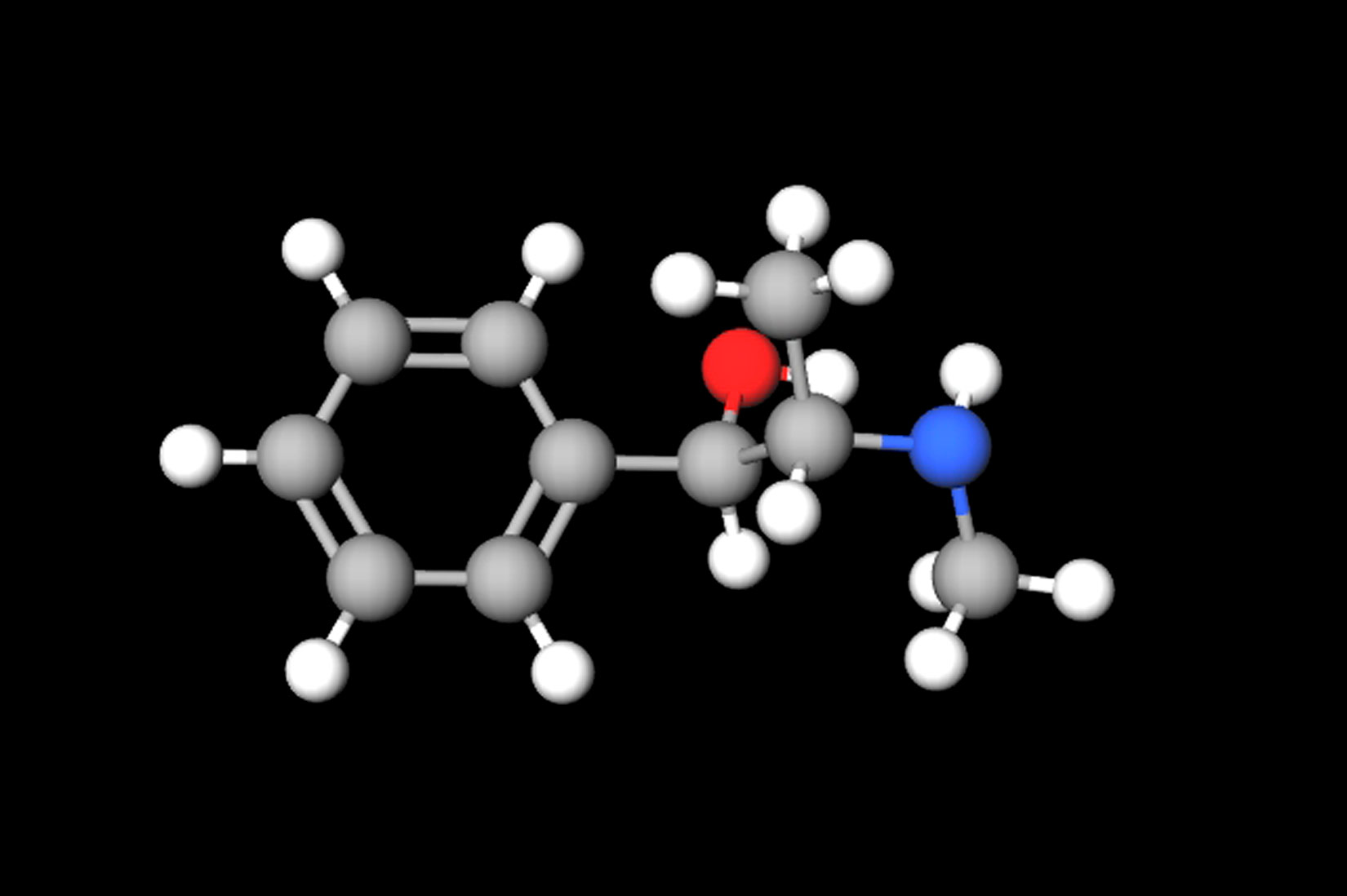
- Efedrin je lijek za plućne bolesti, sužava krvne žile i pomaže kod alergija. Nalazi se u sastavu biljke kositrenice (lat. Ephedra vulgaris) koja se u kineskoj medicini koristi od davnina.
- BHT (2,6-ditertbutil-4-metilfenol) najpoznatiji je antioksidans koji sprečava kvarenje masti u prehrambenim proizvodima (čips, trajni kruh, kobasice, pahuljice od žitarica).
- TNT (trinitrotoluen) otrovna je žuta čvrsta tvar bez mirisa i pripada jakim eksplozivima. Najviše je korišten tijekom II. svjetskog rata, a danas se koristi kao građevinski eksploziv.
Na kraju…
Areni su svuda oko nas, u hrani, odjeći, pa čak i u zraku. Koriste se za proizvodnju brojnih tvari bez kojih život današnjih ljudi ne bi bio toliko lagodan. Tijekom povijesti ljudski je rod katkad bio nesmotren što bi dovelo do tragičnog ishoda te opasno utjecalo na ekološku ravnotežu.
Pronađite povijesnu priču o diklordifeniltrikloretanu (DDT), kemijskom spoju sa slavnim početkom (njegovo je otkriće donijelo Nobelovu nagradu za medicinu), ali čije je korištenje na kraju zabranjeno, iako je spasio više života nego bilo koja druga tvar.
Klikom odaberite jedan ili više točnih odgovora.
Odaberite sve točne odgovore.
Benzen je (dva su odgovora točna):
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Izbacite netočnu tvrdnju.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Kako glasi molekulska formula naftalena?
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Produkti oksidacije (gorenja) benzena uz dovoljan pristup kisika jesu:
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Ulijemo u epruvetu malo benzena i vodenu otopinu kalijeva permanganata. Nakon mućkanja sadržaja epruvete, razdvoje se slojevi tekućina, ali boja otopine kalijeva permanganata ostaje ista kao na početku.
Želite li pokušati ponovo?