Kemijske promjene, osnove kemijskog računa i stehiometrija kemijskih reakcija
- primijeniti matematičke vještine za stehiometrijske izračune
- primijeniti kemijsku terminologiju i simboliku za opisivanje sastava tvari
- analizirati kemijske promjene na primjerima reakcija anorganskih i organskih tvari
- analizirati izmjenu energije između sustava i okoline
- razvijati sposobnost rješavanja problema
- razvijati i poticati svijesti o važnosti ekonomične i ekološki prihvatljive uporabe kemikalija
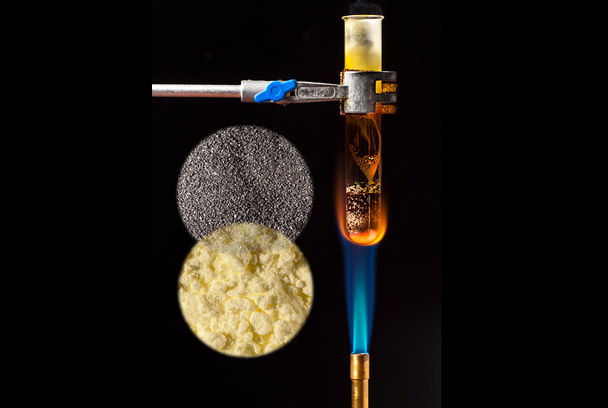
Kemijska analiza i sinteza
Polazeći od primjera iz svakodnevnoga života, na temelju pokusa, digitalnih i multimedijalnih edukativnih priloga upoznajte neke primjere kemijskih reakcija sinteze i analize. Pri rješavanju zadataka služite se digitalnim alatom Pisanje kemijskih jednadžbi na webu.

Ireverzibilne i reverzibilne reakcije
Polazeći od primjera iz svakodnevnoga života, na temelju pokusa usvojite važne značajke ireverzibilnih i reverzibilnih kemijskih promjena. Pri rješavanju zadataka služite se digitalnim alatom Pisanje kemijskih jednadžbi na webu.

Egzotermne i endotermne reakcije
Polazeći od primjera iz svakodnevnoga života, na temelju pokusa proširite svoja znanja iz osnovne škole o energijskim promjenama koje se zbivaju pri kemijskim reakcijama. Pri rješavanju zadataka služite se digitalnim alatom Pisanje kemijskih jednadžbi na webu.

Uvod u kemijski račun
Sadržaji DOS jedinice koreliraju sa sadržajima Matematike i Fizike. Polazište za svladavanje osnova kemijskoga računa temelji se na razumijevanju odnosa između mjernih jedinica, njihova pretvaranja i ispravne uporabe u računskim zadatcima. Riješeni primjeri koji povezuju svakodnevno iskustvo sa sadržajima Kemije bit će vam ogledni za primjenu, povezivanje i kombiniranje potrebnih matematičkih izraza u rješavanju jednostavnih stehiometrijskih problema.

Množina tvari
S obzirom na to da su atomi i molekule vrlo mali, kemičari pri izvođenju kemijskih reakcija ne mogu raditi s pojedinačnim atomima ili molekulama, nego rade s mjerljivim količinama tvari, tj. s uzorcima koji sadržavaju velik broj jedinki. Spoznajte stoga važnost mola – jedne od sedam osnovnih jedinica Međunarodnog sustava jedinica.
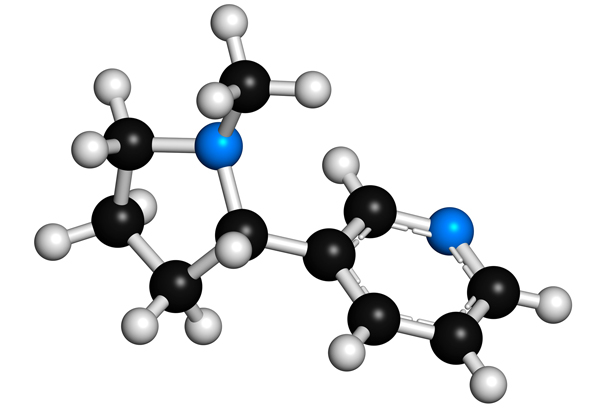
Određivanje empirijske i molekulske formule spoja
Riješeni primjeri i zadatci različitih razina interaktivnosti omogućit će vam razumijevanje informacija ključnih za empirijsku formulu (iskazuje od kojih se vrsta atoma spoj sastoji te koji je najmanji cjelobrojni omjer u kojem ti atomi tvore spoj) i molekulsku formulu (točno iskazuje od koliko se i od kojih atoma sastoji molekula nekoga spoja).

Stehiometrija kemijskih reakcija
Prethodno stečena znanja temeljena na zakonu o očuvanju mase primijenite u razumijevanju pojma stehiometrija kemijske reakcije. Uočite važnost mjerodavnog reaktanta u postavljanju odnosa množina između reaktanata i produkata u kemijskoj reakciji.

Ponavljanje i usustavljivanje gradiva o osnovama kemijskog računa
Primijenite stečeno znanje iz Kemije i povežite ga s osnovnim znanjem iz Matematike u izjednačavanju odnosa množina tvari i kemijskome računu.

