Egzotermne i endotermne reakcije
- objasniti egzotemne i endotermne procese
- razlikovati egzotermne od endotermnih procesa na temelju promjene temperature sustava i okoline tijekom kemijske reakcije
- navesti primjere egzotermnih i endotermnih kemijskih promjena
Uvod
Energija je pratilac svake kemijske reakcije, bilo da je za kemijsku reakciju valja dovesti ili da se reakcijom oslobađa.
Prisjetite se što ste u osnovnoj školi učili o energijskim promjenama tijekom kemijskih reakcija (vidite jedinicu 4.3 Kemijske reakcije i energija u DOS-u Kemija 7).
Egzotermne reakcije
Kalcijev oksid je bijela čvrsta tvar.
Burno reagira s vodom.
Tom reakcijom nastaje čvrsti kalcijev hidroksid ili gašeno vapno, uz oslobađanje topline.
Kalcijev oksid u zdjelici predstavlja otvoreni reakcijski sustav.
Sve izvan toga je okolina.
Jednadžba kemijske reakcije je:
U suvišku vode nastaje bijela i gusta heterogena smjesa.
Ta se smjesa zove vapneno mlijeko.
Dodatkom pijeska nastaje žbuka.
Ako se iz sustava oslobađa energija u okolinu,
tada nastaju produkti koji su energijom siromašniji od reaktanata.
Takve reakcije nazivamo egzotermnim reakcijama.
U energijskom dijagramu na višoj energijskoj razini nalaze se reaktanti.
Na nižoj energetskoj razini nalaze se produkti reakcije.
Kalcijev oksid je bijela čvrsta tvar koja burno reagira s vodom, pri čemu nastaje čvrsti kalcijev hidroksid ili gašeno vapno, uz oslobađanje topline. Kalcijev oksid u zdjelici predstavlja otvoreni reakcijski sustav. Sve izvan toga je okolina.
Jednadžba kemijske reakcije je:
U suvišku vode nastaje bijela i gusta heterogena smjesa, vapneno mlijeko, a dodatkom pijeska nastaje žbuka.
Ako se iz sustava energija oslobađa u okolinu, tada nastaju produkti koji su energijom siromašniji od reaktanata i takve reakcije nazivamo egzotermnim reakcijama.
U energijskom se dijagramu na višoj energijskoj razini nalaze reaktanti, a na nižoj produkti reakcije.
Primjeri
Endotermne reakcije
Žarenjem kalcijeva karbonata nastao je kalcijev oksid ili živo vapno.
Kalcijev karbonat pri sobnoj je temperaturi postojan.
Pri temperaturi oko 700 °C raspada se na
čvrsti kalcijev oksid i plinoviti ugljikov(IV) oksid.
Jednadžba kemijske reakcije je:
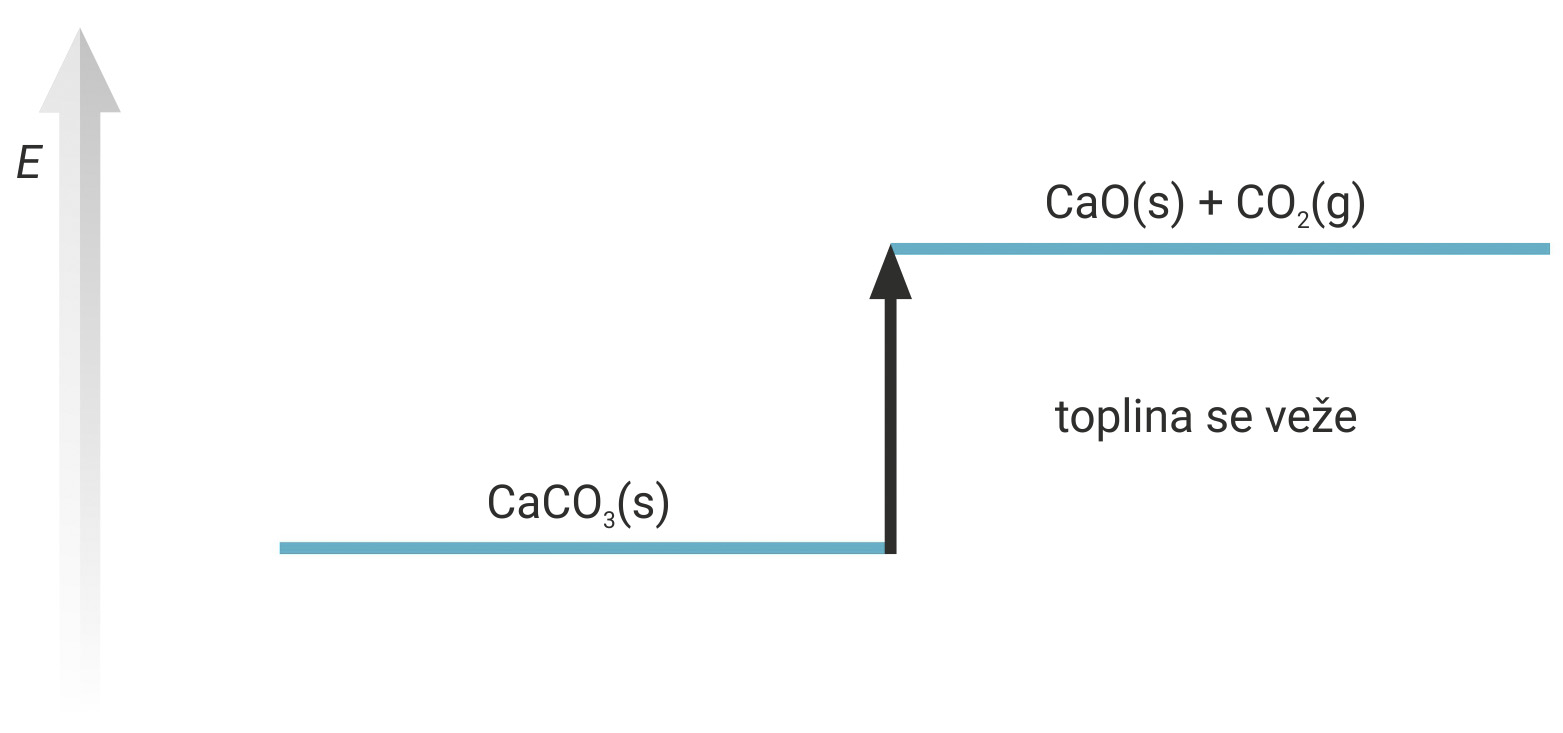
Ako reaktantima dovodimo energiju,
produkti postaju bogatiji energijom od reaktanata.
Sustav veže energiju iz okoline.
Takve reakcije nazivamo endotermnim reakcijama.
Žarenjem kalcijeva karbonata nastao je kalcijev oksid ili živo vapno.
Kalcijev karbonat pri sobnoj je temperaturi postojan, a pri temperaturi od oko 700 °C raspada se na čvrsti kalcijev oksid i plinoviti ugljikov(IV) oksid.
Jednadžba kemijske reakcije je:
Za odvijanje reakcije nužno je dovoditi energiju. Kad je ukupna energija nastalih produkata veća od ukupne energije reaktanta, takve reakcije nazivamo endotermnim reakcijama.
Primjeri
Na kraju…
Rješavanjem interaktivnog kviza ponovite pojmove vezane uz kemijsku reakciju.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Željezo burno reagira s klorom, pri tome nastaje žuto-smeđa čvrsta tvar, željezov(III) klorid. Označite ispravno napisanu kemijsku jednadžbu:

Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Odaberite reakcije sinteze:
A
B
C
D
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Kisik se laboratorijski dobiva zagrijavanjem kalijeva klorata. Koja jednadžba prikazuje taj proces?
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Fotoliza je reakcija:
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Reakcija izgaranja magnezija na zraku primjer je:
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Koji grafički prikaz energijskih dijagrama odgovara reakciji gorenja magnezija?
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?