Tekućine i njihova karakteristična svojstva
- opisati svojstva tvari u tekućem agregacijskom stanju
- navesti što su tekućine
- razlikovati neka svojstva tekućina
- analizirati fazni dijagram vode
Uvod
Koje su sličnosti, a koje razlike tvari u čvrstom, tekućem i plinovitom stanju?
Uvod
Koje su sličnosti, a koje razlike tvari u čvrstom, tekućem i plinovitom stanju?
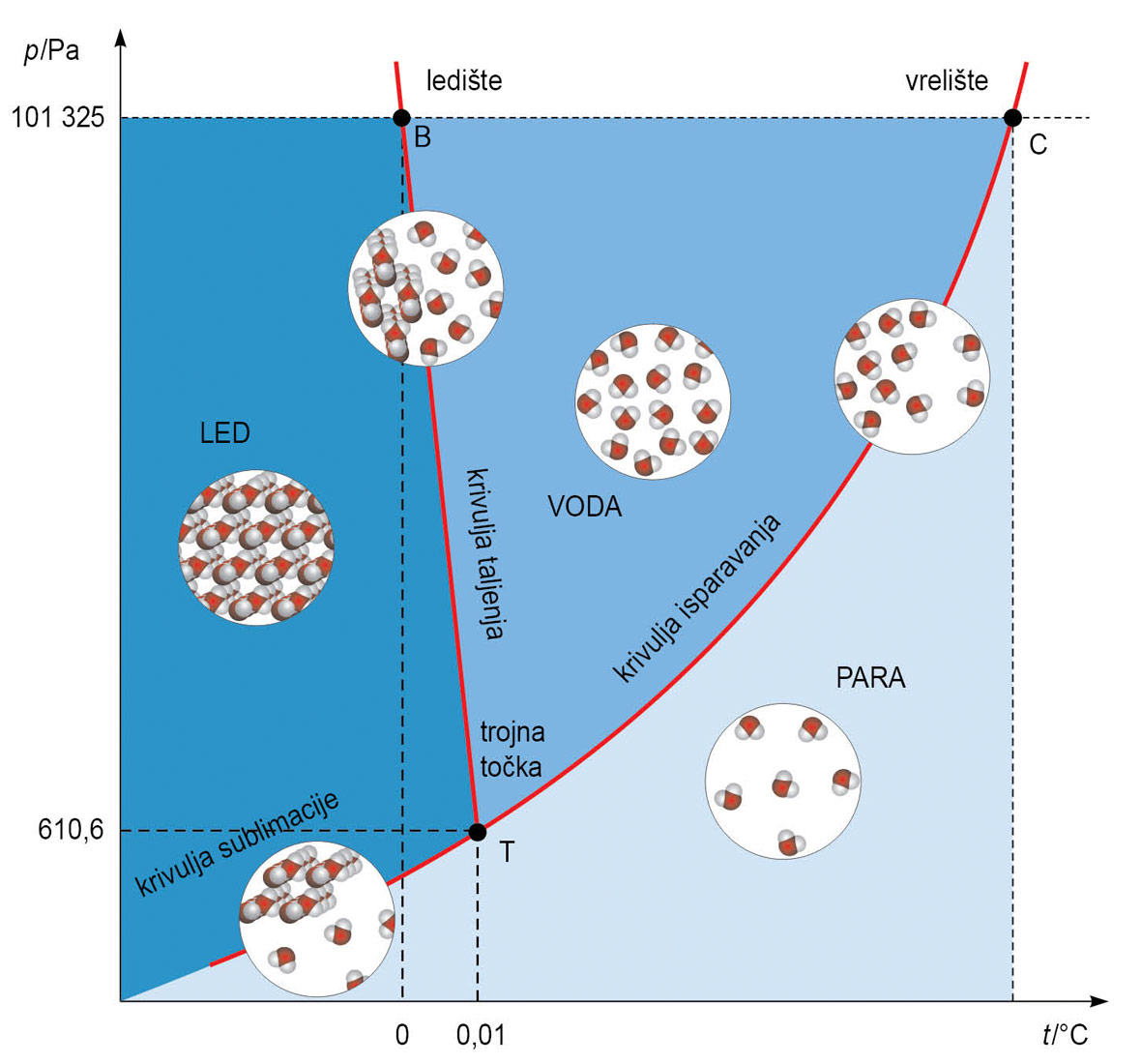
Uspostavljanje ravnoteže između pojedinih agregacijskih stanja ili faza nekog sustava pri određenom tlaku i temperaturi, uz pretpostavku stalnoga volumena, može se prikazati faznim dijagramom (p, t).
Uspostavljanje ravnoteže između pojedinih agregacijskih stanja ili faza nekog sustava pri određenom tlaku i temperaturi, uz pretpostavku stalnoga volumena, može se prikazati
Unesite odgovore na pripadajuća mjesta.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Granice faza su ravnotežne krivulje u faznom dijagramu.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Krivulja isparavanja predstavlja skup točaka u kojima pri određenoj temperaturi i tlaku, voda i led su u ravnoteži.
Krivulja isparavanja predstavlja skup točaka u kojima su pri određenoj temperaturi i tlaku voda i vodena para u ravnoteži.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Pri 20 °C voda može biti samo u tekućoj fazi.
Osim o temperaturi, faza vode ovisi i o tlaku.
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
U trojnoj točci u ravnoteži su:
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Granice faza su ravnotežne krivulje u faznom dijagramu.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Krivulja isparavanja predstavlja skup točaka u kojima su pri određenoj temperaturi i tlaku voda i led u ravnoteži.
Krivulja isparavanja predstavlja skup točaka u kojima su pri određenoj temperaturi i tlaku voda i vodena para u ravnoteži.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Pri 20 °C voda može biti samo u tekućoj fazi.
Osim o temperaturi, faza vode ovisi i o tlaku.
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
U trojnoj točci u ravnoteži su:
Želite li pokušati ponovo?
Tvari u tekućem agregacijskom stanju imaju manji (<) stupanj uređenosti strukture od tvari u čvrstom agregacijskom stanju.
Između čestica u tekućini udaljenost je veća (>) zbog slabijih privlačnih sila.
Zato se čestice u tekućini relativno slobodno gibaju i lako mijenjaju položaj.
Tekućine poprimaju oblik posude u kojoj se nalaze.
Nestlačive su, tj. povećanjem tlaka ne mijenjaju volumen.
Što su tekućine?
Tekućine su tvari koje su pri sobnoj temperaturi u tekućem agregacijskom stanju.
Umjesto uobičajenoga naziva tekućina za tvar u tekućem agegacijskom stanju rabi se i naziv kapljevina.
Takvo agregacijsko stanje naziva se kapljevitim.
Naziv tekućina (engl. fluid) tada ima šire značenje i obuhvaća:
- kapljevine (engl. liquid)
- plinove (engl. gas).
Osnovna svojstva tekućina ovise o privlačnim silama između čestica u tekućini.
Tvari u tekućem agregacijskom stanju imaju manji stupanj uređenosti strukture od tvari u čvrstom agregacijskom stanju. Između čestica u tekućini udaljenost je veća zbog slabijih privlačnih sila. Zato se čestice u tekućini relativno slobodno gibaju i lako mijenjaju položaj. Tekućine poprimaju oblik posude u kojoj se nalaze i nestlačive su tj. povećanjem tlaka ne mijenjaju volumen.
Što su tekućine?
Tekućine su tvari koje su pri sobnoj temperaturi u tekućem agregacijskom stanju. Umjesto uobičajenoga naziva tekućina za tvar u tekućem agegacijskom stanju rabi se i naziv kapljevina, a takvo agregacijsko stanje naziva se kapljevitim. Naziv tekućina (engl. fluid) tada ima šire značenje i obuhvaća: kapljevine (engl. liquid) i plinove (engl. gas).
Osnovna svojstva tekućina ovise o privlačnim silama između čestica u tekućini.
| Vrste privlačnih sila | primjer | jakost međudjelovanja kj/mol |
|---|---|---|
| ion-dipol | Na+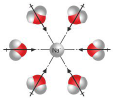 |
40 – 600 |
| dipol-dipol | i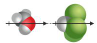 |
5 – 25 |
| vodikova-veza | i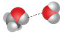 |
10 – 40 |
| ion-inducirani dipol | i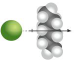 |
3 – 15 |
| dipol-inducirani dipol | i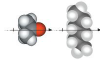 |
2 – 10 |
| Londonove sile ili disperzijske sile | i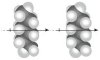 |
0,05 – 40 |
Svojstva po kojima tekućine možemo razlikovati su primjerice:
- gustoća,
- viskoznost,
- napetost površine i
- tlak pare.
Svojstva po kojima tekućine možemo razlikovati su primjerice: gustoća, viskoznost, napetost površine i tlak pare.
Gustoća tekućina
Vjerojatno ste primijetili da vam je lakše plivati u moru, nego u bazenu sa slatkom vodom, kao i da kapljice aromatičnog ulja plivaju na površini kupke za kupanje.
Ogromne sante leda plivaju na površini mora ili rijeka.
Kockica leda pliva u čaši na površini osvježavajućeg soka.
Koji je razlog tomu?
Gustoća tekućina
Vjerojatno ste primijetili da vam je lakše plivati u moru, nego u bazenu sa slatkom vodom, kao i da kapljice aromatičnog ulja plivaju na površini kupke za kupanje. Ogromne sante leda plivaju na površini mora ili rijeka, kao što i kockica leda pliva u čaši na površini osvježavajućeg soka. Koji je razlog tomu?
Razlog svega što smo naveli su različite gustoće navedenih tvari.
Od ranije znamo:
Oznaka za gustoću je grčko slovo ρ (čitati ro).
Mjerna jedinica u SI sustavu je kg m3 (čitati kilogram po metru kubičnom).
Pretvorba mjerne jedinice za gustoću
Razlog svega što smo naveli različite su
Oznaka za gustoću je grčko slovo ρ (čitati ro), a mjerna jedinica u SI sustavu je kg m-3.
Pretvorba mjerne jedinice za gustoću
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Koliki je obujam (V) 1000 kg (m) leda?
ρ (leda) = 900 kg/m3
m (leda) = 1000 kg
V (leda) = ?
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Koliki je obujam 1000 kg leda ako je gustoća leda 0,900 g/cm3?
Želite li pokušati ponovo?
Istraživački zadatak
U menzuru od 500 mL oprezno se uz stijenku ulije po:
100 mL meda, vode, ulja, metanola pazeći pri tom da se slojevi ne pomiješaju.
U tako napunjenu menzuru ubace se sljedeće tvari:
guma, komadić mramora, lego kockica, stiropor i pluteni čep.
| tvar | pri 25 °C | tvar | pri 25 °C |
| med | 1,435 | guma | 1,171 |
| voda | 1,000 | mramor | 2,850 |
| ulje | 0,920 | plastična masa | 0,850 |
| metanol | 0,792 | stiropor | 0,049 |
| pluto | 0,249 |

Odgovorite na pitanja:
- Koje svojstvo navedenih tekućina određuje redosljed njihovog ulijevanja u menzuru?
- Gdje se u menzuri nalaze ubačeni predmeti?
Potvrdu svog odgovora potražite na slici!
Odgovori:
- Redoslijed ulijevanja tekućina u menzuru određuje gustoća tekućine (ρ).
- Ubacivanjem predmeta različite gustoće komadić mramora pao je na dno jer mu je gustoća (ρ) veća (>) od gustoće (ρ) meda.
- Guma pliva na medu.
- Lego kockica pliva na vodi.
- Stiropor i pluteni čep plutaju na metanolu.
Istraživački zadatak
U menzuru od 500 mL oprezno se uz stijenku ulije po 100 mL meda, vode, ulja i metanola pazeći pri tom da se slojevi ne pomiješaju. U tako napunjenu menzuru ubace se sljedeće tvari: guma, komadić mramora, lego kockica (plastična masa), stiropor i pluteni čep.
| tvar | pri 25 °C | tvar | pri 25 °C |
| med | 1,435 | guma | 1,171 |
| voda | 1,000 | mramor | 2,850 |
| ulje | 0,920 | plastična masa | 0,850 |
| metanol | 0,792 | stiropor | 0,049 |
| pluto | 0,249 |
 Tvari različitih gustoća
Tvari različitih gustoća
Odgovorite na pitanja:
- Koje svojstvo navedenih tekućina određuje redosljed njihovog ulijevanja u menzuru?
- Gdje se u menzuri nalaze ubačeni predmeti? Potvrdu svog odgovora potražite na slici!
Odgovori:
- Redoslijed ulijevanja tekućina u menzuru određuje gustoća tekućine.
- Ubacivanjem predmeta različite gustoće komadić mramora pao je na dno jer mu je gustoća veća od gustoće meda. Guma pliva na medu, lego kockica na vodi, a stiropor i pluteni čep plutaju na metanolu.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Riješeni primjer 1
Odredite gustoću mlijeka, etanola i benzina na temelju eksperimentalno dobivenih vrijednosti. Koristeći literaturne (teoretske) vrijednosti za gustoće navedenih tekućina, izračunajte i relativne pogreške mjerenja.
Korak 1.
Izvagane su prazne menzure, a vrijednosti njihovih masa (m1) upisane su u tablicu podataka.
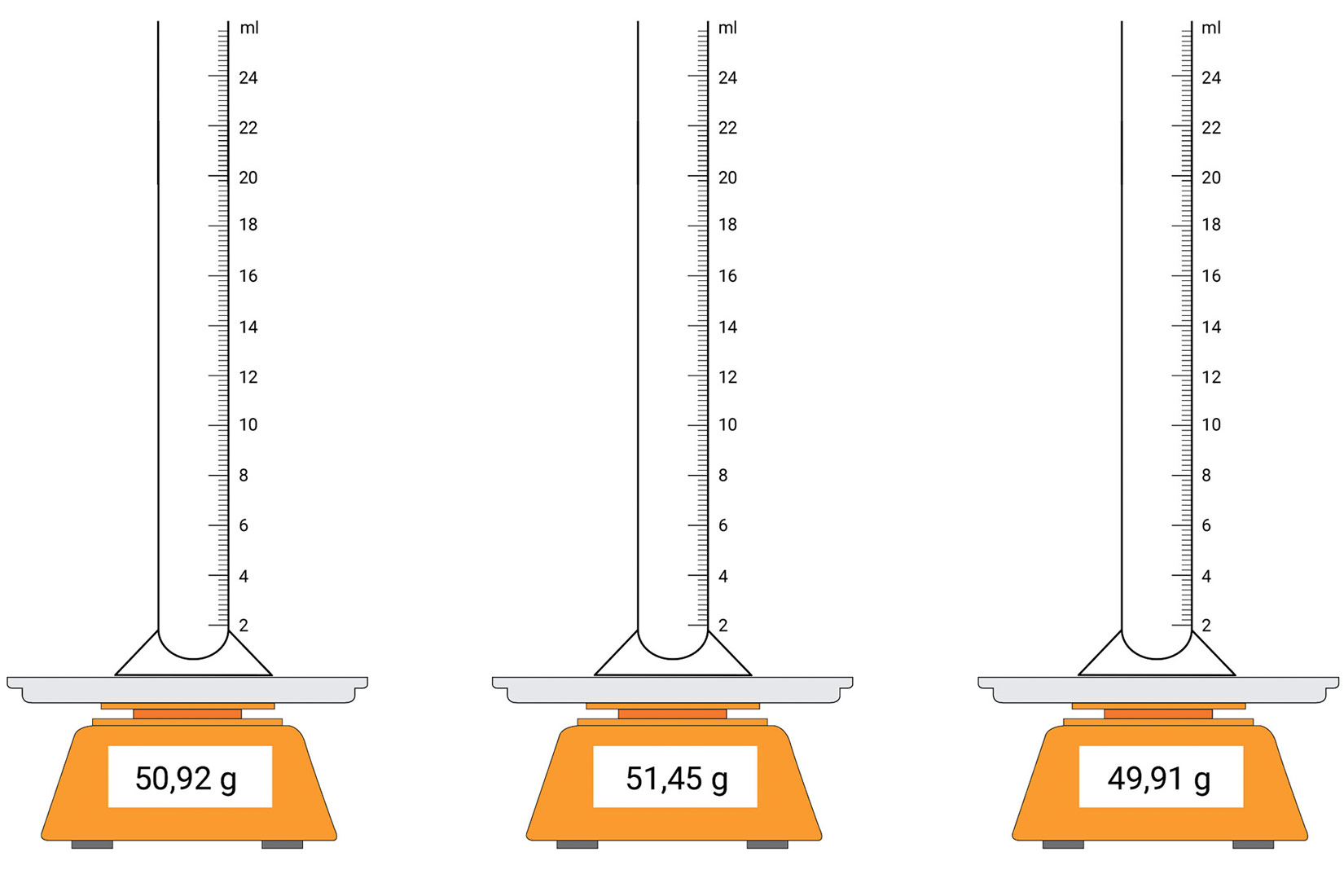
Korak 2.
U menzurama se s lijeva na desno nalazi: mlijeko, etanol i benzin. Na temelju slike odčitane su vrijednosti volumena (V) navedenih tekućina i upisane u tablicu.
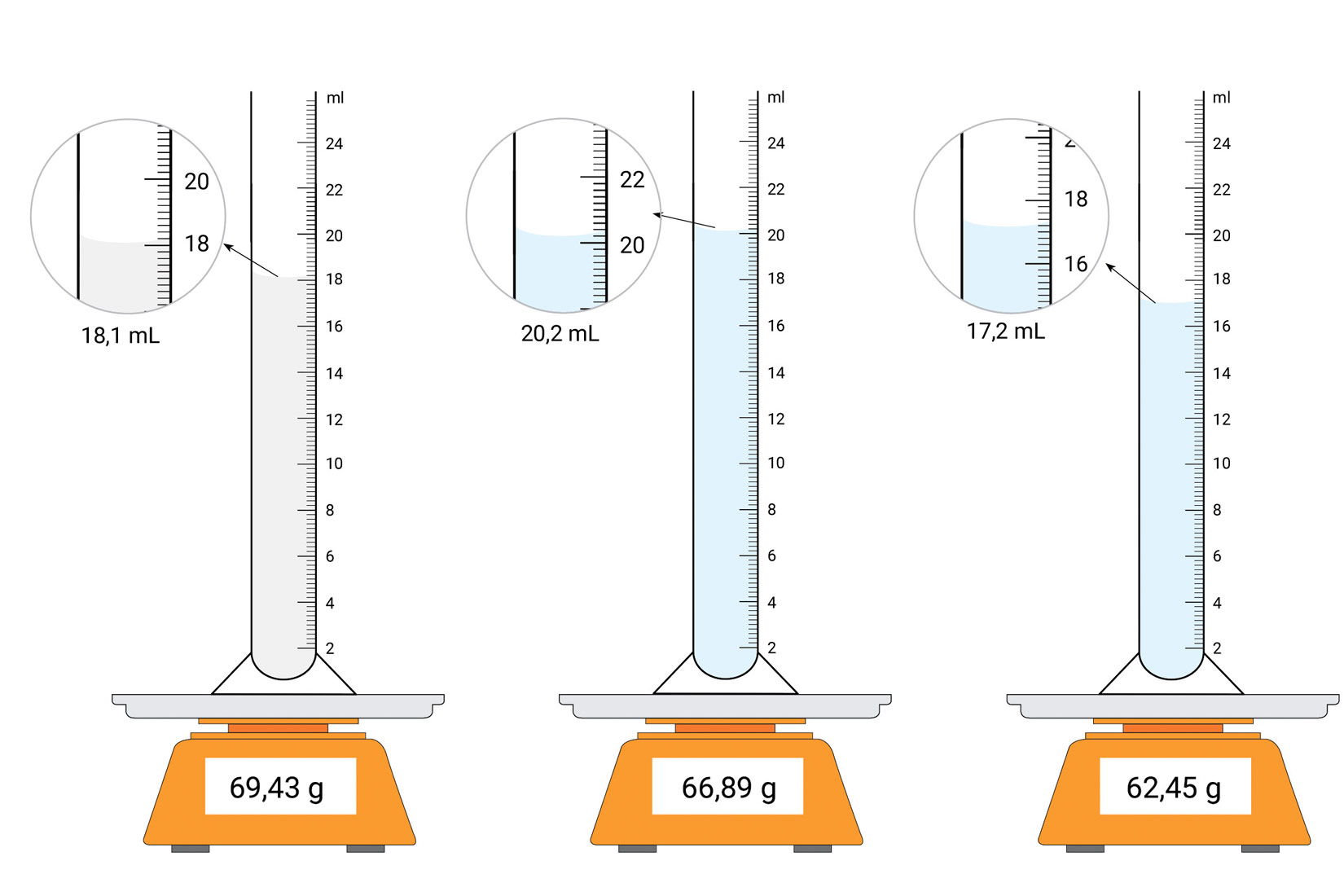
Iz slike se može odčitati i masa pojedine menzure i tekućine koja se u njoj nalazi (m2).
Mase mlijeka, etanola i benzina (m3) izračunate su na temelju izraza:
m3 = m2 – m1.
Dobivene su vrijednosti također upisane u tablicu podataka.
| m1/g | m2/g | m3/g | V(tekućine)/cm3 | ρE(tekućine)/g cm–3 | ρL(tekućine)/g cm–3 | P/% | |
|---|---|---|---|---|---|---|---|
| mlijeko | 50,92 | 69,43 | 18,51 | 18,1 | |||
| alkohol | 51,45 | 66,89 | 15,44 | 20,2 | |||
| benzin | 49,91 | 62,45 | 12,54 | 17,2 |
Korak 3.
Iz dobivenih podataka izračunate su eksperimentalno dobivene vrijednosti za gustoće mlijeka, etanola i benzina, ρE(tekućine).
Kako je za zadane tekućine poznat podatak njihovih literaturnih (teoretskih) vrijednosti gustoća, ρL(tekućine), mogu se izračunati relativne pogreške mjerenja, P, prema sljedećoj formuli:
P – relativna pogreška mjerenja
ρE – eksperimentalno određena gutoća
ρL – literaturna (teoretska) vrijednost gustoće
Odgovor:
Eksperimentalno određena gustoća mlijeka iznosi 1,02 g cm–3, etanola 0,764 g cm–3 i benzina 0,729 g cm–3.
Relativne pogreške mjerenja su intervalu od 0,5 do 3,0 %.
| m1/g | m2/g | m3/g | V(tekućine)/cm3 | ρE(tekućine)/g cm–3 | ρL(tekućine)/g cm–3 | P/% | |
|---|---|---|---|---|---|---|---|
| mlijeko | 50,92 | 69,43 | 18,51 | 18,1 | 1,02 | 1,030 | 0,68 |
| etanol | 51,45 | 66,89 | 15,44 | 20,2 | 0,764 | 0,789 | 3,17 |
| benzin | 49,91 | 62,45 | 12,54 | 17,2 | 0,729 | 0,708 | 2,97 |
Određivanje gustoće (ρ) pomoću areometra temelji se na Arhimedovu zakonu.
Određivanje gustoće pomoću areometra temelji se na Arhimedovu zakonu.
Na temelju istraživačkog miniprojekta, radom u skupinama, istražite kada i gdje se rodio Arhimed, čime se bavio i što ga je navelo da iz kade istrči gol vičući: „Eureka!“.
Pretražite mrežne stranice po ključnim pojmovima, npr. gustoća čvrstih tvari (vidi 1. razred), gustoća tekućina, ovisnost gustoće o temperaturi, areometar.
Unutar skupine u alatu Xmind načinite mentalnu mapu.
Pomoću mentalne mape usustavite ključne pojmove.
Svoje uratke predstavite suučenicima u razredu.
Izaberite najkreativniju i najbolje usustavljenu mentalnu mapu.
Ne zaboravite istražiti i umetnuti u mentalnu mapu i neke zanimljivosti iz života i rada Arhimeda.
Na temelju istraživačkog miniprojekta, radom u skupinama, istražite kada i gdje se rodio Arhimed, čime se bavio i što ga je navelo da iz kade istrči gol vičući: „Eureka!“.
Pretražite mrežne stranice po ključnim pojmovima, npr. gustoća čvrstih tvari (vidi 1. razred), gustoća tekućina, ovisnost gustoće o temperaturi, areometar. Unutar skupine u alatu Xmind načinite mentalnu mapu i na taj način usustavite ključne pojmove.
Svoje uratke predstavite suučenicima u razredu. Izaberite najkreativniju i najbolje usustavljenu mentalnu mapu. Ne zaboravite istražiti i umetnuti u mentalnu mapu i neke zanimljivosti iz života i rada Arhimeda.
Viskoznost
Viskoznost je karakteristično svojstvo tekućina.
Definira se kao unutarnje trenje između slojeva u tekućinama.
Unutarnje trenje posljedica je međumolekulskih sila (vodikove veze,
).
Jakost privlačnih sila ovisi o obliku molekula kao i o njihovoj veličini.
Ulje je viskoznija tekućina od vode, jer su ulja (jestiva ili motorna) građena od dugačkih nepolarnih ugljikovodičnih lanaca.
Molekule vode su vrlo male i kuglastog oblika.
Viskoznost
Viskoznost je karakteristično svojstvo tekućina, definira se kao unutarnje trenje između slojeva u tekućinama. Unutarnje trenje posljedica je međumolekulskih sila (vodikove veze,
Više informacija o međumolekulskim interakcijama možete pronaći u jedinici 3.2 Međumolekulske interakcije u DOS-u Kemija 1.
Ulje je viskoznija tekućina od vode, jer su ulja (jestiva ili motorna) građena od dugačkih nepolarnih ugljikovodičnih lanaca, a molekule vode su vrlo male i kuglastog oblika.
Tekućine različite viskoznosti
Oznaka za
je grčko slovo η (čitati eta).
Mjerna jedinica SI sustava je Pa s
(čitati paskal sekunda).
Proučite sliku koja prikazuje brzinu istjecanja slojeva u tekućini.
Oznaka za
Proučite sliku koja prikazuje brzinu istjecanja slojeva u tekućini.
Koji slojevi imaju najveću, a koji najmanju brzinu istjecanja?
Najsporije će istjecati sloj uz stijenku cijevi.
Najbrže će istjecati sloj koji je najudaljeniji od stijenke – sloj koji istječe kroz sredinu cijevi.
Različite brzine istjecanja slojeva tekućine posljedica su trenja tekućine sa stijenkama cijevi i trenja između slojeva tekućine koji se međusobno dodiruju i gibaju.
Koji slojevi imaju najveću, a koji najmanju brzinu istjecanja?
Najsporije će istjecati sloj uz stijenku cijevi, a najbrže sloj koji je najudaljeniji od stijenke – sloj koji istječe kroz sredinu cijevi. Različite brzine istjecanja slojeva tekućine posljedica su trenja tekućine sa stijenkama cijevi i trenja između slojeva tekućine koji se međusobno dodoruju i gibaju.
Hoće li na viskoznost tekućine utjecati oblik i veličina molekula?
Usporedite strukture molekula:
a) etanola,
b) etilen- glikola,
c) propan-1-ola,
d) glicerola.
Hoće li na viskoznost tekućine utjecati oblik i veličina molekula?
Usporedite strukture molekula: a) etanola b) etilen-glikola
c) propan-1-ola i d) glicerola.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Viskoznost ima važnu ulogu u različitim područjima ljudske djelatnosti npr. u proizvodnji složenih motornih ulja (ljetna i zimska ulja), tekstilnoj industriji, proizvodnji različitih uljnih boja i dr.
Površinska napetost
Površinska napetost je sila koja nastaje zbog različitog okruženja čestica na površini i u unutrašnjosti tekućine.
Svaka čestica u unutrašnjosti tekućine u cijelosti je okružena s istovrsnim česticama.
Nasuprot tome, čestica na površini s jedne strane je u dodiru s istovrsnim česticama, a s druge strane je u dodiru sa česticama zraka.
U slučaju vode, sile između molekula u unutrašnjosti su jake vodikove veze.
Okruženje molekula vode na površini i u unutrašnjosti.
Viskoznost ima važnu ulogu u različitim područjima ljudske djelatnosti npr. u proizvodnji složenih motornih ulja (ljetna i zimska ulja), tekstilnoj industriji, proizvodnji različitih uljnih boja i dr.
Više informacija o viskoznosti možete pronaći u jedinici 5.5 Strujanje fluida u DOS-u Fizika 1.
Površinska napetost
Površinska napetost je sila koja nastaje zbog različitog okruženja čestica na površini i u unutrašnjosti tekućine. Svaka čestica u unutrašnjosti tekućine u cijelosti je okružena s istovrsnim česticama. Nasuprot tome, čestica na površini s jedne strane je u dodiru s istovrsnim česticama, a s druge strane je u dodiru sa česticama zraka. U vodi, sile između molekula u unutrašnjosti su jake vodikove veze.
Za razliku od njih, u površinskom sloju djeluju vrlo slabe sile između molekula vode i molekula zraka.
Time što molekule iz unutrašnjosti nastoje privući molekule s površine, površina se ponaša kao elastična opna koja nastoji smanjiti površinu tekućine.
Površinska napetost je naziv za silu koja održava ovu elastičnu opnu.
Oznaka za napetost površine je grčko slovo σ
(čitati sigma).
Mjerna jedinica je Nm–1 (čitati njutn po metru).
Napetost površine ovisi o jakosti privlačnih sila između molekula i o temperaturi.
Za razliku od njih, u površinskom sloju djeluju vrlo slabe sile između molekula vode i molekula zraka. Time što molekule iz unutrašnjosti nastoje privući molekule s površine, površina se ponaša kao elastična opna koja nastoji smanjiti površinu tekućine. Površinska napetost je naziv za silu koja održava ovu elastičnu opnu.
Oznaka za
Napetost površine ovisi o jakosti privlačnih sila između molekula i o temperaturi.

Kuglice i kapi
Čestice na površini tekućine imaju nešto višu energiju.
Zbog toga tekućine teže tomu da im površina bude što manja.
Iz geometrije vam je poznato da kugla ima najmanji omjer površine (P) i volumena (V).
Iz fizike vam je poznato da je kugla energijski najstabilniji oblik.
Zbog toga tekućine teže poprimiti oblik kugle pa je površina tekućine u posudi zakrivljena ploha.
Zakrivljena ploha naziva se menisk.
Ploha može biti konkavna ili konveksna.
To se dobro vidi u epruveti ili još bolje u kapilari.
U prirodi zbog djelovanja sile teže, kuglice tekućine pretvaraju se u kapi (kiša, suze….).

Kuglice i kapi
Čestice na površini tekućine imaju nešto višu energiju, pa zbog toga tekućine teže tomu da im površina bude što manja.
Iz geometrije vam je poznato da kugla ima najmanji omjer površine i volumena, a iz fizike da je kugla energijski najstabilniji oblik.
Zbog toga tekućine teže poprimaju oblik kugle, pa je površina tekućine u posudi zakrivljena ploha koju se naziva menisk.
Ploha može biti konkavna ili konveksna što se dobro vidi u epruveti ili još bolje u kapilari.
U prirodi zbog djelovanja sile teže, kuglice tekućine pretvaraju se u kapi (kiša, suze….).
Zbog čega se površine vode i žive u epruvetama razlikuju?
Voda u staklenoj epruveti prijanja uz staklo zbog sila adhezije (sile između raznovrsnih čestica) između vode i stakla.
Sile adhezije su jače od sila kohezije (sile između istovrsnih čestica) između molekula vode.
Gornja površina vode, menisk, svijen prema gore, ploha je konkavna.
Kod žive je međutim menisk savijen prema dolje, gdje živa dodiruje staklo pa je ploha konveksna.
U ovom slučaju sile kohezije između atoma žive puno su jače od sila adhezije između žive i stakla.
Voda u staklenoj epruveti prijanja uz staklo zbog sila adhezije (sile između raznovrsnih čestica) između vode i stakla, koje su jače od sila kohezije (sile između istovrsnih čestica) između molekula vode. Gornja površina vode, menisk, savijen prema gore, ploha je konkavna.
Kod žive je međutim menisk savijen prema dolje, gdje živa dodiruje staklo, pa je ploha konveksna. U ovom slučaju sile kohezije između atoma žive puno su jače od sila adhezije između žive i stakla.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Izvedite kod kuće jednostavni pokus kojim ćete dokazati da je površinska napetost vode velika.
Tijek pokusa fotografirajte i fotografije posložite u prezentaciju koju možete načiniti u nekom od alata koji su vam dostupni u CARNETovom e-Laboratoriju.
Istražite što će se dogoditi, ako u zdjelicu dodate kap detergenta ili tekućega sapuna.
Izvedite kod kuće jednostavni pokus kojim ćete dokazati da je površinska napetost vode velika. Tijek pokusa fotografirajte i fotografije posložite u prezentaciju koju možete načiniti u nekom od alata koji su vam dostupni u CARNETovom e-Laboratoriju.
Istražite što će se dogoditi, ako u zdjelicu dodate kap detergenta ili tekućega sapuna.
Što može smanjiti površinsku napetost tekućina?
Površinska napetost tekućine ovisi o:
- jakosti privlačnih sila između molekula u tekućini,
- prirodi tvari s kojom tekućina graniči i
- temperaturi.
Površinska napetost vode može se, osim povišenjem temperature, smanjiti i dodavanjem površinski aktivnih tvari (tenzidi), primjerice sapuna ili deterdženta.
Djelovanje sapuna i deterdženta može se objasniti građom njihovih molekula.
Sapuni su natrijeve ili kalijeve soli viših masnih kiselina, primjerice, oleinske C17H33COOH i stearinske C17H35COOH.
Anionski dio sapuna ima:
- hidrofobni dio (“rep”)
- hidrofilni dio (“glava”).
Kation je .
Što može smanjiti površinsku napetost tekućina?
Površinska napetost tekućine ovisi o jakosti privlačnih sila između molekula u tekućini, o prirodi tvari s kojom tekućina graniči i o temperaturi.
Površinska napetost vode može se osim povišenjem temperature smanjiti i dodavanjem površinski aktivnih tvari (tenzidi) primjerice, sapuna ili deterdženta.
Djelovanje sapuna i deterdženta može se objasniti građom njihovih molekula.
Sapuni su natrijeve ili kalijeve soli viših masnih kiselina, primjerice, oleinske i stearinske kiseline.
Anionski dio sapuna ima hidrofobni dio (“rep”) i hidrofilni dio (“glava”). Kation je .
Kako sapun uklanja masne mrlje?
Navedena građa sapuna omogućuje uklanjanje masnih mrlja pri pranju tako da nepolarni ugljikovodični repovi okružuju nepolarne kapljice masti.
Polarna glava se okreće prema polarnim molekulama vode.
Na taj način nastaju micele čija je površina polarne građe.
To omogućuje njihovo raspršivanje u vodi i na taj način ispiranje nečistoća.
Kako sapun uklanja masne mrlje?
Navedena građa sapuna omogućuje uklanjanje masnih mrlja pri pranju tako da nepolarni ugljikovodični repovi okružuju nepolarne kapljice masti, a polarna glava se okreće prema polarnim molekulama vode. Na taj način nastaju micele čija je površina polarne građe, što omogućuje njihovo raspršivanje u vodi i na taj način ispiranje nečistoća.
Tlak para
Zašto se znojimo?
Zašto nas znoj hladi?
Poznato je da je znojenje tjelesni mehanizam za hlađenje tijela kada smo izloženi visokim temperaturama.
Molekule tekućine u dodiru s kožom apsorbiraju toplinu koja prelazi u kinetičku energiju (Ek).
To omogućava isparavanje koje je povezano s utroškom topline pa zato imamo osjećaj hlađenja.
Tekućine na zraku isparavaju, tj. spontano prelaze iz tekućeg u plinovito agregacijsko stanje.
Prema tome, iznad tekućine se uvijek nalazi neki broj molekula u pari što uzrokuje tlak pare tekućine.
|
octena kiselina |
voda |
etanol |
aceton |
|
| 20 | 1,56 | 2,33 | 5,85 | 24,58 |
| 30 | 2,75 | 4,24 | 10,50 | 37,68 |
| 50 | 7,55 | 12,33 | 29,62 | 81,62 |
Služeći se digitalnim alatom Avogadro prikažite modele molekula octene kiseline (CH3COOH), vode (H2O), etanola (C2H5OH) i acetona (CH3COCH3) sastavljene od kuglica i štapića.
Na temelju tabličnih podataka odgovorite na sljedeća pitanja.
Tlak para
Zašto se znojimo i zašto nas znoj hladi? Poznato je da je znojenje tjelesni mehanizam za hlađenje tijela kada smo izloženi visokim temperaturama. Molekule tekućine u dodiru s kožom apsorbiraju toplinu koja prelazi u kinetičku energiju i omogućava isparavanje koje je povezano s utroškom topline pa zato imamo osjećaj hlađenja.
Tekućine na zraku isparavaju, tj. spontano prelaze iz tekućeg u plinovito agregacijsko stanje. Prema tome, iznad tekućine se uvijek nalazi neki broj molekula u pari što uzrokuje tlak pare tekućine.
|
octena kiselina |
voda |
etanol |
aceton |
|
| 20 | 1,56 | 2,33 | 5,85 | 24,58 |
| 30 | 2,75 | 4,24 | 10,50 | 37,68 |
| 50 | 7,55 | 12,33 | 29,62 | 81,62 |
Služeći se digitalnim alatom Avogadro prikažite modele molekula octene kiseline, vode, etanola i acetona sastavljene od kuglica i štapića.
Na temelju tabličnih podataka odgovorite na sljedeća pitanja.
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Povećanjem temperature (T) tlak pare tekućine raste.
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Je li tvrdnja točna ili netočna? Odaberite klikom na gumb.
Je li ova tvrdnja točna?
Povećanjem temperature tlak pare tekućine raste.
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Brzina isparavanja tekućina povećava se s porastom temperature.
Razlog tome je što pri višim temperaturama veći (>) broj molekula ima dovoljnu kinetičku energiju (Ek) za napuštanje tekućine.
Dakle, pri višoj temperaturi veća (>) je brzina isparavanja i veći (>) tlak pare tekućine.
Na početku isparavanja u pari je malo čestica koje se sudarima mogu vratiti u tekućinu – kondenzirati.
Zagrijavanjem je sve veći broj čestica u pari kao i onih koje se kondenzacijom vraćaju u tekućinu.
Kada se broj čestica koje isparavanjem izlaze iz tekućine izjednači s brojem čestica koje se kondenzacijom vraćaju u tekućinu kaže se da je uspostavljena dinamička ravnoteža.
Dinamička se ravnoteža može postići samo u zatvorenom sustavu.
Tlak pare iznad tekućine u stanju dinamičke ravnoteže naziva se ravnotežnim tlakom pare.
Vrijednost ravnotežnog tlaka pare pokazatelj je relativne jakosti međumolekulnih interakcija u tekućinama.
Vrijednost ravnotežnog tlaka pare ovisi o temperaturi i o prirodi tvari.
Kada se tlak pare u tekućini izjednači s vanjskim tlakom, tekućina vrije.
Temperaturu pri kojoj je tlak para tekućine jednak vanjskom tlaku nazivamo vrelištem.
Vrelište čiste vode pri normalnom atmosferskom tlaku od 101 325 Pa je 100 °C.
Brzina isparavanja tekućina povećava se s porastom temperature jer pri višim temperaturama veći broj molekula ima dovoljnu kinetičku energiju za napuštanje tekućine. Dakle, pri višoj temperaturi veća je brzina isparavanja i veći tlak pare tekućine.
Na početku isparavanja u pari je malo čestica koje se sudarima mogu vratiti u tekućinu – kondenzirati, no zagrijavanjem je sve veći broj čestica u pari kao i onih koje se kondenzacijom vraćaju u tekućinu.
Kada se broj čestica koje isparavanjem izlaze iz tekućine izjednači s brojem čestica koje se kondenzacijom vraćaju u tekućinu kaže se da je uspostavljena dinamička ravnoteža. Dinamička se ravnoteža može postići samo u zatvorenom sustavu.
Tlak pare iznad tekućine u stanju dinamičke ravnoteže naziva se ravnotežnim tlakom pare. Vrijednost ravnotežnog tlaka pare pokazatelj je relativne jakosti međumolekulskih interakcija u tekućinama, a osim o prirodi tvari ovisi i o temperaturi.
Kada se tlak pare u tekućini izjednači s vanjskim tlakom, tekućina vrije. Temperaturu pri kojoj je tlak para tekućine jednak vanjskom tlaku nazivamo vrelištem. Vrelište čiste vode pri normalnom atmosferskom tlaku od 101 325 Pa je 100 °C.

Zašto ekspres lonci skraćuju vrijeme kuhanja?
U ekspres loncu hrana se kuha pod povećanim tlakom.
Zašto je brže skuhana?
Zašto na Mt. Everestu voda vrije na oko 76 °C pa je potrebno dulje vrijeme za kuhanje hrane?
Utjecaj tlaka na vrelište objašnjava zašto ekspress lonci štede vrijeme u kuhinji.
Ekspres lonci pod tlakom su zatvoreni i dopuštaju pari da iziđe samo kad prijeđe određeni tlak.
Tlak iznad vode u loncu čine atmosferski tlak i tlak pare.
Stoga, voda (H2O) vrije iznad 100 °C i hrana u takvom loncu će biti izložena višoj temperaturi i brže će se skuhati.

Zašto ekspres lonci skraćuju vrijeme kuhanja?
U ekspres loncu hrana se kuha pod povećanim tlakom.
Zašto je brže skuhana? Zašto na Mt. Everestu voda vrije na oko , pa je potrebno dulje vrijeme za kuhanje hrane?
Utjecaj tlaka na vrelište objašnjava zašto ekspress lonci štede vrijeme u kuhinji. Ekspres lonci pod tlakom su zatvoreni i dopuštaju pari da iziđe samo kad prijeđe određeni tlak. Tlak iznad vode u loncu čine atmosferski tlak i tlak pare. Stoga, voda vrije iznad i hrana u takvom loncu će biti izložena višoj temperaturi i brže će se skuhati.
Na kraju…
Proučite prikaze triju grafikona.
Odgovorite kako se mijenjaju gustoća, koeficijent napetosti površine i viskoznosti destilirane vode u ovisnosti o temperaturi.
Na kraju…
Proučite prikaze triju grafikona i odgovorite kako se mijenjaju gustoća, koeficijent napetosti površine i viskoznosti destilirane vode u ovisnosti o temperaturi.