Ravnotežna konstanta ionizacije vode i pH-vrijednost
- objasniti ravnotežnu konstantu ionizacije vode,
- izračunati pH i pOH-vrijednosti vodenih otopina
- odabrati indikatore za kiseline i lužine
- objasniti važnost pH-vrijednosti vodenih otopina u svakodnevnom životu
Uvod
U reakciji s kiselinama molekule vode su proton akceptori.
U reakciji s bazama molekule vode su proton donori .
Poznata je činjenica da kemijski čista voda slabo provodi električnu struju jer je koncentracija iona u njoj vrlo mala.
Kako nastaju ioni u kemijski čistoj vodi?
Ionski produkt vode
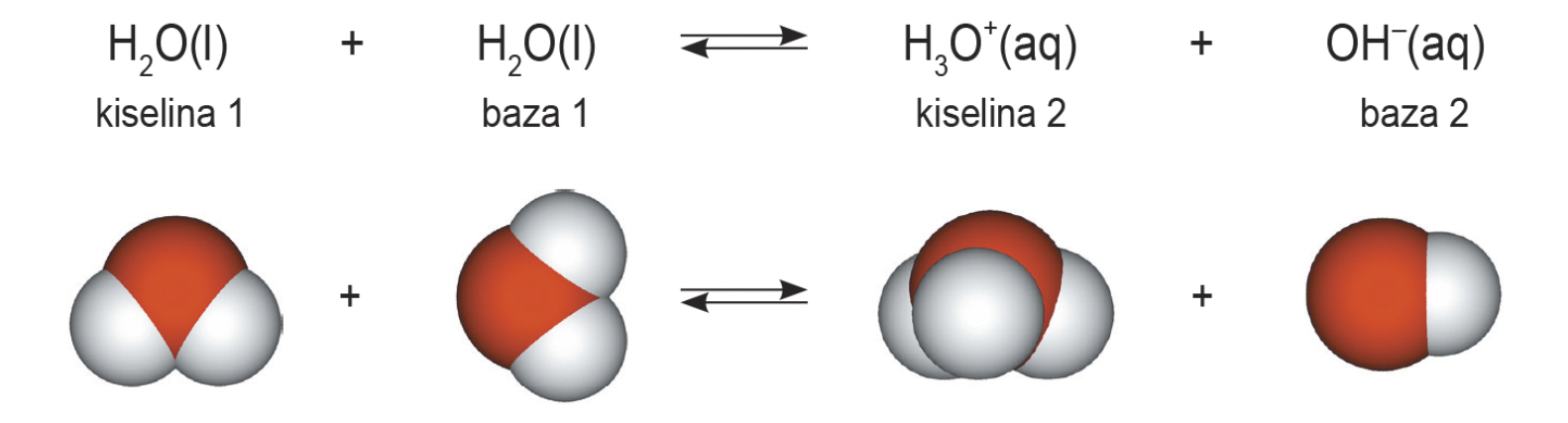
U čistoj se vodi nalazi vrlo mali broj oksonijevih () i hidroksidnih () iona koji nastaju pri prijelazu protona s jedne molekule vode na drugu.
Uvod
U reakciji s kiselinama molekule vode su proton akceptori , a u reakciji s bazama proton donori .
Poznata je činjenica da kemijski čista voda slabo provodi električnu struju jer je koncentracija iona u njoj vrlo mala.
Kako nastaju ioni u kemijski čistoj vodi?
Ionski produkt vode
U čistoj se vodi nalazi vrlo mali broj oksonijevih i hidroksidnih iona koji nastaju pri prijelazu protona s jedne molekule vode na drugu.
U gornjoj reakciji ravnoteža je pomaknuta prema molekulama vode.
U ovoj su reakciji molekule vode i proton-donori i proton-akceptori.
U čistoj vodi samo jedna od 107 molekula vode podliježe autoprotolizi.
Budući da u reakciji sudjeluju molekule vode, u izraz za ravnotežnu konstantu ionizacije vode uvrštava se množinski udio za vodu, x (H2O).
Za jako razrijeđene vodene otopine vrijedi:
x (H2O)≈ 1.
Prema tome izraz za ravnotežnu konstantu ionizacije vode (Kc) je:
Umnožak (∙) ravnotežne konstante ionizacije (Kc) vode i kvadrirane vrijednosti množinskog udjela vode daje novu konstantu, konstantu ionskog produkta vode, Kw.
Indeks w dolazi od engleske riječi za vodu – water.
Iz navedenoga može se zaključiti da je konstanta ionskoga produkta vode, , određena umnoškom (•) ravnotežnih množinskih koncentracija oksonijevih i hidroksidnih iona.
U gornjoj reakciji ravnoteža je pomaknuta prema molekulama vode. U ovoj su reakciji molekule vode i proton-donori i proton-akceptori. Kada su istovrsne molekule u reakciji i proton-donori i proton-akceptori takve reakcije nazivamo autoprotoliza. U čistoj vodi samo jedna od molekula vode podliježe autoprotolizi.
Budući da u reakciji sudjeluju molekule vode, u izraz za ravnotežnu konstantu ionizacije vode, uvrštava se množinski udio za vodu, x(H2O).
Za jako razrijeđene vodene otopine vrijedi da je x(H2O)≈ 1. Prema tome izraz za ravnotežnu konstantu ionizacije vode je:
Umnožak ravnotežne konstante ionizacije vode i kvadrirane vrijednosti množinskog udjela vode daje novu konstantu, konstantu ionskog produkta vode, , (indeks w dolazi od engleske riječi za vodu – water).
Iz navedenoga može se zaključiti da je konstanta ionskoga produkta vode, , određena umnoškom ravnotežnih množinskih koncentracija oksonijevih i hidroksidnih iona.
Vrijednost ravnotežne konstante ionizacije vode je eksperimentalno određena i pri 25 °C iznosi:
Koncentracije oksonijevih (H3O+) i hidroksidnih (OH–) iona u čistoj vodi su jednake (=).
Pri 25 °C iznose .
Vrijednost ravnotežne konstante ionizacije vode je eksperimentalno određena i pri 25 °C iznosi:
Koncentracije oksonijevih i hidroksidnih iona u čistoj vodi su jednake i pri 25 °C iznose .
| °C | |
|---|---|
| 0 | |
| 15 | |
| 25 | |
| 37 | |
| 40 | |
| 60 |
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Ravnotežna konstanta ionizacije vode iskazana na drugi način
Ravnotežna konstanta ionizacije (Kw) vode može se izraziti i kao umnožak (•) konstante ionizacije kiseline (Ka) i konstante ionizacije baze (Kb).
Pokažimo na primjeru!
Za reakciju:
Amonijev ion (NH4+) je u reakciji konjugirana kiselina.
Reagira s vodom prema reakciji:
Dobivene izraze za ravnotežne koncentracije oksonijevih (H3O+) i hidoksidnih iona (OH–) uvrstimo u izraz za ravnotežnu konstantu ionskoga produkta vode (Kw):
Ravnotežna konstanta ionizacije vode iskazana na drugi način
Ravnotežna konstanta ionizacije vode može se izraziti i kao umnožak konstante ionizacije kiseline i konstante ionizacije baze.
Pokažimo na primjeru!
Za reakciju:
Amonijev ion je u reakciji konjugirana kiselina i reagira s vodom prema reakciji:
Dobivene izraze za ravnotežne koncentracije oksonijevih i hidoksidnih iona uvrstimo u izraz za ravnotežnu konstantu ionskoga produkta vode:
Riješite zadatak!
Izračunajte konstantu ionizacije konjugirane kiseline, , u reakciji amonijaka s vodom, ako je .
Rješenje: Ka(NH4+) = 5,6 × 10–10 mol dm–3
pH – vrijednost kao mjera kiselosti otopina
Danski biokemičar S. P. L. Sørensen [čitaj Sernsen] (1909.) uveo je pojam pH-vrijednosti (čitaj pe-ha).
Pojam pH-vrijednosti uveo je zbog vrlo malih množinskih koncentracija (c) oksonijevih ⦋H3O+⦎ i hidroksidnih iona ⦋OH–⦎,
pH-vrijednost se definira kao negativni logaritam (– log) brojčane vrijednosti množinske koncentracije (c) oksonijevih iona ⦋H3O+⦎.
Dakle, može se reći da pH vrijednost na kodirani način daje informaciju o množinskoj koncentraciji (c) oksonijevih iona ⦋H3O+⦎ u jako razrijeđenoj vodenoj otopini.
pOH – vrijednost se definira kao negativni logaritam (– log) brojčane vrijednosti množinske koncentracije (c) hidroksidnih iona ⦋OH–⦎.
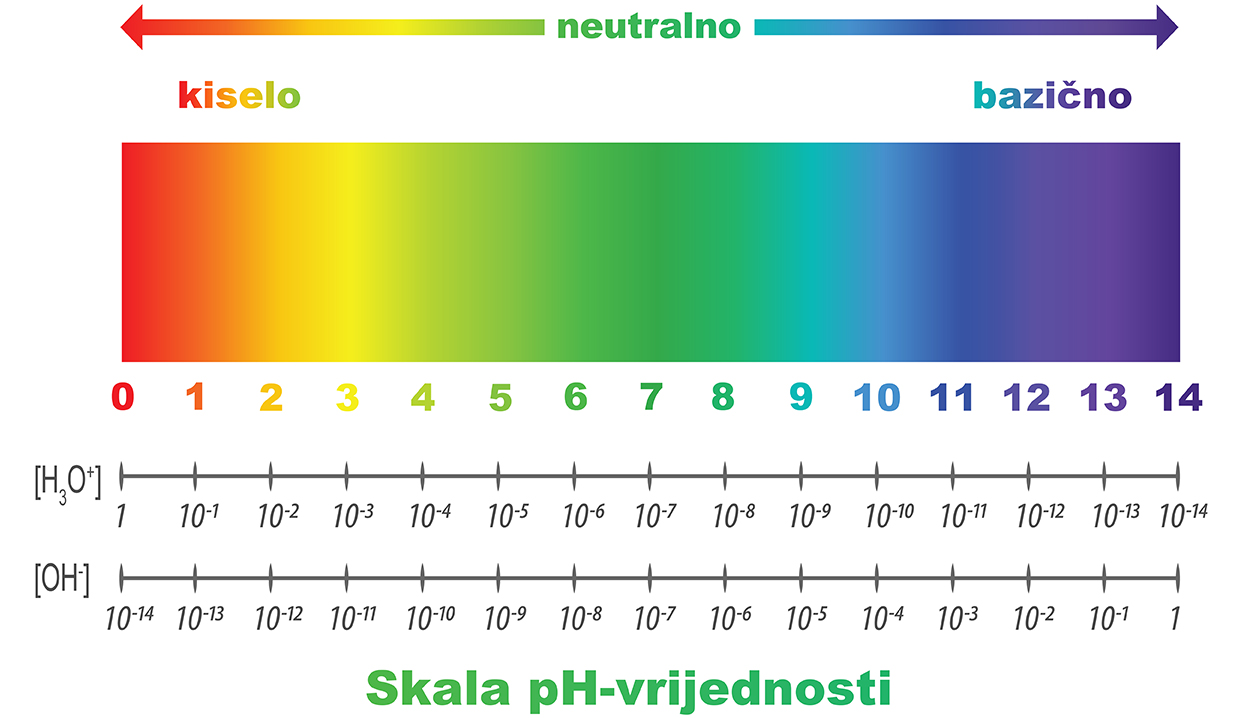
U kiselim otopinama koncentracije oksonijevih iona ⦋H3O+⦎ su veće (>) od 10–7 mol dm–3.
To znači da je pH-vrijednost kiselih otopina manja (<) od 7.
U bazičnim otopinama koncentracije oksonijevih iona ⦋H3O+⦎ su manje (<) od 10–7 mol dm–3.
To znači da je pH-vrijednost bazičnih otopina veća (>) od 7.
Za vodene otopine pri 25 °C vrijedi:
pH + pOH = 14
U destiliranoj vodi pri 25 °C koncentracije oksonijevih ⦋H3O+⦎ i hidroksidnih iona ⦋OH–⦎ su jednake (=).
One iznose 1,0 × 10–7 mol dm–3.
pH-vrijednost kao mjera kiselosti otopina
Zbog vrlo malih množinskih koncentracija oksonijevih i hidroksidnih iona u vodenim otopinama, danski biokemičar S. P. L. Sørensen [Sernsen] 1909. godine uveo je pojam pH-vrijednosti (čitaj pe-ha).
pH-vrijednost se definira kao negativni logaritam brojčane vrijednosti množinske koncentracije oksonijevih iona.
Dakle, može se reći da
pOH-vrijednost se definira kao negativni logaritam brojčane vrijednosti množinske koncentracije hidroksidnih iona.
U kiselim su otopinama koncentracije oksonijevih iona veće od , što znači da je pH-vrijednost kiselih otopina manja od 7.
U bazičnim otopinama koncentracije oksonijevih iona su manje od , što znači da je pH-vrijednost bazičnih otopina veća od 7.
Za vodene otopine pri 25 °C vrijedi:
U destiliranoj vodi pri 25 °C koncentracije oksonijevih i hidroksidnih iona su jednake i iznose .
pH – vrijednost može imati bilo koju vrijednost na ljestvici od 0 do 14.
Neutralne otopine imaju pH 7.
Kisele otopine imaju pH od 0 do 7.
Bazične otopine imaju pH od 7 do 14.
| kisele otopine | neutralne otopine | bazične otopine |
|---|---|---|
pH-vrijednost može imati bilo koju vrijednost na ljestvici od 0 do 14. Neutralne otopine imaju pH = 7, kisele otopine od 0 do 7, a bazične otopine od 7 do 14.
| kisele otopine | neutralne otopine | bazične otopine |
|---|---|---|
Za precizno mjerenje pH-vrijednosti otopina koristi se pH-metar.
Za precizno mjerenje pH-vrijednosti otopina koristi se pH-metar.
Indikatori
Je li otopina kisela, neutralna ili bazična, može se odrediti:
- pH-metrom
- pomoću indikatora.
Indikatori su najčešće slabe organske kiseline ili baze.
Svojstvo tvari koja može poslužiti kao indikator je da se struktura njezine molekule mijenja ovisno o mediju u kojem se nalazi:
- u neutralnom
- u kiselom
- u lužnatom mediju
| + | + | ||||||
| ↓ | ↓ | ||||||
| kiseli oblik indikatora | bazični oblik indikatora | ||||||
Indikatori koji mijenjaju boju u točno određenom pH-području zovu se kiselo-bazni indikatori.
Mnoge tvari se koriste kao kiselo-bazni indikatori.
Najpoznatiji među njima su:
- I. lakmus
- II. univerzalni indikator
- III. metiloranž
- IV. fenolftalein.
Mnoge biljke sadrže u staničnim organelima biljne pigmente: klorofil (zeleno), ksantofil (žuto), karotenoid (narančast) i drugi koji mogu biti indikatori kiselosti ili lužnatosti.
Pigmenti antocijanini (crveni, plavi i ljubičasti) daju boju:
- plodovima trešnje, crnog i crvenog grožđa
- cvjetovima hibiskusa, ljubičice
- listovima crvenoga kupusa.
Indikatori
Je li otopina kisela, neutralna ili bazična, može se odrediti osim pH-metrom i pomoću indikatora.
Indikatori su najčešće slabe organske kiseline ili baze. Svojstvo tvari koja može poslužiti kao indikator je da se struktura njezine molekule mijenja ovisno o mediju u kojem se nalazi – u neutralnom, kiselom ili u lužnatom.
| + | + | ||||||
| ↓ | ↓ | ||||||
| kiseli oblik indikatora | bazični oblik indikatora | ||||||
Indikatori koji mijenjaju boju u točno određenom pH-području zovu se kiselo-bazni indikatori.
Mnoge tvari se koriste kao kiselo-bazni indikatori, a najpoznatiji među njima su lakmus, univerzalni indikator, metiloranž i fenolftalein.
Mnoge biljke sadrže u staničnim organelima biljne pigmente: klorofil (zeleno), ksantofil (žuto), karotenoid (narančast) i drugi koji mogu biti indikatori kiselosti ili bazičnosti.
Pigmenti antocijanini (crveni, plavi i ljubičasti) daju boju plodovima trešnje, crnog i crvenog grožđa, cvjetovima hibiskusa, ljubičice, te listovima crvenoga kupusa.

Biljke kao kiselo-bazni indikatori
Mnoge biljke, odnosno biljni pigmenti, u prirodi djeluju kao indikatori kiselosti ili lužnatosti.
Riješite istraživački zadatak dostupan na izvoru 1 i otkrijte koje su to biljke.

Biljke kao kiselo-bazni indikatori
Mnoge biljke, odnosno biljni pigmenti, u prirodi djeluju kao indikatori kiselosti ili lužnatosti. Riješite istraživački zadatak dostupan na izvoru 1 i otkrijte koje su to biljke.
Upoznajmo najčešće indikatore!
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Vodena otopina pri 25 °C ima pH = 8.
Koncentracija hidroksidnih iona (OH–) je :
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Vodena otopina pri 25 °C ima pH = 8. Koncentracija hidroksidnih iona je:
Unesite odgovore na pripadajuća mjesta.
Želite li pokušati ponovo?
pH-vrijednosti otopina jakih kiselina i jakih baza
Jake kiseline i jake baze disociraju u vodi gotovo potpuno, pa vrijedi:
c (H3O+) = c (jake kiseline)
c (OH–) = c (jake baze)
| fromula | naziv |
|---|---|
| perklorna | |
| odovodična | |
| bromovodična | |
| klorovodična | |
| sumporna | |
| dušična |
| fromula | naziv |
|---|---|
| cezij hidroksid | |
| rubidij hidroksid | |
| kalij hidroksid | |
| natrij hidroksid | |
| litij hidroksid | |
| barijev hidroksid | |
| stroncij hidroksid | |
| kalcijev hidroksid |
pH-vrijednosti otopina jakih kiselina i jakih baza
Jake kiseline i jake baze ioniziraju u vodi gotovo potpuno, pa vrijedi:
| kiseline | baze | ||
|---|---|---|---|
| ime | formula | ime | formula |
| perklorna kiselina | rubidijev hidroksid | ||
| jodovodična kiselina | kalijev hidroksid | ||
| bromovodična kiselina | natrijev hidroksid | ||
| klorovodična kiselina | barijev hidroksid | ||
| sumporna kiselina | stroncijev hidroksid | ||
| dušična kiselina | kalcijev hidroksid | ||
Riješeni primjer 1
Izračunajte pH-vrijednost otopine dušične kiseline .
Množinska koncentracija (c) dušične kiseline iznosi 1,50×10−5 mol dm−3.
Zadano je:
c (HNO3) = 1,50×10−5 mol dm−3
Traži se:
pH = ?
Postupak:
Ionizacija dušične kiseline
Budući da je dušična kiselina
jaka kiselina, potpuno ionizira u vodi.
Iz toga proizlazi da je množinska koncentracija (c) oksonijevih iona
(H3O+) jednaka (=) množinskoj koncentraciji (c) dušične kiseline .
pH = 4,82
Odgovor:
pH – vrijednost otopine dušične kiseline je 4,82.
Riješeni primjer 1.
Izračunajte pH-vrijednost otopine dušične kiseline množinske koncentracije .
Zadano je:
Traži se:
pH = ?
Postupak:
Ionizacija dušične kiseline:
Budući da je dušična kiselina jaka kiselina, potpuno ionizira u vodi iz čega proizlazi da je množinska koncentracija oksonijevih iona jednaka množinskoj koncentraciji dušične kiseline.
pH = 4,82
Odgovor:
pH-vrijednost otopine dušične kiseline je 4,82.
Riješeni primjer 2
Izračunajte pH-vrijednost otopine kalijeve lužine (KOH) množinske koncentracije (c) .
Zadano je:
c
Traži se:
pH = ?
Postupak:
Disocijacija kalijeve hidroksida (KOH):
Budući da je kalijeva lužina (KOH) jaka lužina, potpuno disocira u vodi.
Množinska koncentracija (c) hidroksidnih iona ( ) jednaka (=) je množinskoj koncentraciji (c) kalijeve lužine ( ).
pOH = 0,592
pH = 13,4
Odgovor:
pH – vrijednost kalijeve lužine ( ) je 13,4.
Riješeni primjer 2.
Izračunajte pH-vrijednost otopine kalijeve lužine množinske koncentracije .
Zadano je:
Traži se:
pH = ?
Postupak:
Disocijacija kalijeva hidroksida:
Budući da je kalijeva lužina jaka lužina, potpuno disocirana u vodi, množinska koncentracija hidroksidnih iona jednaka je množinskoj koncentraciji kalijeve lužine.
pOH = 0,592
pH = 13,4
Odgovor:
pH-vrijednost kalijeve lužine je 13,4.
Riješeni primjer 3
Izračunajte pH – vrijednost otopine barijeve lužine (Ba(OH)2).
Množinska koncentracija (c) barijeve lužine (Ba(OH)2) iznosi 0,256 mol dm−3.
Zadano je:
c
Traži se:
pH = ?
Postupak:
Disocijacija barijeva hidroksida ( ):
Iz reakcije disocijacije barijeve lužine (Ba(OH)2) vidljivo je da je koncentracija (c) hidroksidnih iona (OH–) dva puta (2∙) veća (>) od koncentracije (c) lužine.
c (OH–) = 2 ∙ c
pOH
pOH
pOH = 0,291
pOH
pOH = 13,7
pH – vrijednost barijeve lužine (Ba(OH)2) je 13,7.
Riješeni primjer 3
Izračunajte pH-vrijednost otopine barijeve lužine množinske koncentracije .
Zadano je:
Traži se:
pH = ?
Postupak:
Disocijacija barijeva hidroksida:
Iz reakcije disocijacije barijeve lužine vidljivo je da je koncentracija hidroksidnih iona dva puta veća od koncentracije lužine.
pOH = 0,291
pH = 13,7
Odgovor:
pH-vrijednost barijeve lužine je 13,7.
pH-vrijednosti otopina slabih kiselina i slabih baza
Za slabe kiseline i slabe baze karakteristično je da slabo disociraju u vodi.
Iz toga slijedi da koncentracija (c) oksonijevih iona (H3O+) slabih kiselina nije jednaka (≠) koncentraciji (c) slabih kiselina.
Odnosno, koncentracija (c) hidroksidnih iona (OH–) nije jednaka (≠) koncentraciji (c) slabih baza.
Da bi se izračunala koncentracija (c) oksonijevih iona (H3O+) potreban je podatak za konstantu ionizacije kiseline, Ka, ili stupanj ionizacije, α, slabe kiseline.
Tada je :
ili
Stupanj ionizacije (α) slabih kiselina je omjer množinske koncentracije (c) oksonijevih iona nastalih ionizacijom slabe kiseline i množinske koncentracije (c) kiseline.
Na isti način poznavajući konstantu ionizacije baze (Kb) ili stupanj disocijacije (α) slabe baze može se izračunati koncentracija (c) hidroksidnih iona (OH–).
Stupanj ionizacije (α) slabih baza je omjer množinske koncentracije (c) hidroksidnih iona (OH–) nastalih ionizacijom slabe baze i množinske koncentracije (c) slabe baze.
| Formula | Naziv |
|---|---|
| sumporasta | |
| fosforna | |
| etanska (octena | |
| ugljična | |
| sumporovodična | |
| metanska (mravlja) | |
| dušikasta | |
| hipoklorasta | |
| cijanovodična | |
| fenol |
| Formula | Naziv |
|---|---|
| magnezijeva lužina | |
| amonijak | |
| metil amin | |
| etil amin | |
| anilin |
Za jedinke koje se ponašaju kao kiseline i kao baze, kažemo da su amfoterne.
Primjerice, hidrogenkarbonatni ioni, HCO3−, u reakciji mogu biti i proton-donori i proton-akceptori.
pH-vrijednosti otopina slabih kiselina i slabih baza
Za slabe kiseline i slabe baze karakteristično je da slabo ioniziraju u vodi. Iz toga slijedi da koncentracija oksonijevih iona slabih kiselina nije jednaka koncentraciji slabih kiselina, odnosno koncentracija hidroksidnih iona nije jednaka koncentraciji slabih baza.
Da bi se izračunala koncentracija oksonijevih iona potreban je podatak za konstantu ionizacije kiseline, , ili stupanj ionizacije, , slabe kiseline.
Tada je:
Stupanj ionizacije slabih kiselina je omjer množinske koncentracije oksonijevih iona nastalih ionizacijom slabe kiseline i množinske koncentracije kiseline.
Na isti način poznavajući konstantu ionizacije baze ili stupanj ionizacije slabe baze, , može se izračunati koncentracija hidroksidnih iona.
Tada je :
Stupanj ionizacije slabih baza je omjer množinske koncentracije hidroksidnih iona nastalih ionizacijom slabe baze i množinske koncentracije slabe baze.
Slabe kiseline:
, sumporasta kiselina ; , fosforna kiselina; , etanska (octena) kiselina;
, ugljična kiselina, ; sumporovodična kiselina, ; metanska (mravlja) kiselina; , dušikasta kiselina; , hipoklorasta kiselina; , cijanovodična kiselina; , fenol.
Slabe baze:
, magnezijeva lužina; , amonijak; ,
metilamin; , etilamin; , anilin.
Za jedinke koje se ponašaju kao kiseline i kao baze, kažemo da su amfoterne.
Primjerice, hidrogenkarbonatni ioni, , u reakciji mogu biti i proton-donori i proton-akceptori.
Riješeni primjer 4.
Izračunajte pH-vrijednost octene kiseline ().
Množinska koncentracija (c) octene kiseline () iznosi 0,200 mol dm-3.
Konstanta ionizacije, Ka, octene kiseline (CH3COOH) iznosi 1,80 × 10–5 mol dm-3.
Zadano je:
Traži se:
pH = ?
Postupak:
Ionizacija octene kiseline () prikazana je jednadžbom:
Budući da octena kiselina (CH3COOH) ne ionizira u cijelosti, potrebno je uzeti u obzir konstantu ravnoteže, .
Sljedeća tablica u kojoj analiziramo promjenu koncentracije, pomoći će u postavljanju jednadžbe kojom ćemo izračunati koncentraciju oksonijevih iona (H3O+) potrebnu za konačan izračun pH-vrijednosti.
| početna koncentracija |
0 | 0 | |
|---|---|---|---|
| promjena | |||
| ravnotežna koncentracija |
Tražena jednadžba proizlazi iz definicije konstante ravnoteže.
Kvadratna jednadžba:
ima dva rješenja:
Kemijski, od dva matematički realna rješenja, samo pozitivna (+) vrijednost množinske koncentracije (c) oksonijevih iona (H3O+) ima smisla:
pH-vrijednost navedene otopine je 2,72.
Međutim, jednadžba koju smo upravo riješili, može se pojednostaviti ako se zbog vrlo slabe ionizacije kiseline zanemari smanjenje početne koncentracije kiseline.
Tada umjesto ravnotežne koncentracije računamo s početnom koncentracijom .
Tada rješavanje jednadžbe konstante ravnoteže izgleda ovako:
Na kraju treba izračunati pH-vrijednost:
Odgovor: pH-vrijednost navedene otopine je 2,72.
Riješeni primjer 4.
Izračunajte pH-vrijednost octene kiseline, množinske koncentracije , ako je konstanta ionizacije octene kiseline .
Zadano je:
Traži se:
pH-vrijednost = ?
Izradak:
Ionizacija octene kiseline prikazana je jednadžbom:
Budući da octena kiselina ne ionizira u cijelosti, potrebno je uzeti u obzir konstantu ravnoteže, .
Sljedeća tablica u kojoj analiziramo promjenu koncentracije, pomoći će u postavljanju jednadžbe kojom ćemo izračunati koncentraciju oksonijevih iona, potrebnu za konačan izračun pH-vrijednosti.
| početna koncentracija | 0 | 0 | |
|---|---|---|---|
| promjena | |||
| ravnotežna koncentracija |
Tražena jednadžba proizlazi iz definicije konstante ravnoteže.
Kvadratna jednadžba:
ima dva rješenja:
Kemijski, od dva matematički realna rješenja, samo pozitivna vrijednost množinske koncentracije oksonijevih iona ima smisla:
pH-vrijednost navedene otopine je 2,72.
Međutim, jednadžba koju smo upravo riješili, može se pojednostaviti, ako se zbog vrlo slabe ionizacije kiseline zanemari smanjenje početne koncentracije kiseline. Tada umjesto ravnotežne koncentracije računamo s početnom koncentracijom .
Tada rješavanje jednadžbe konstante ravnoteže izgleda ovako:
Na kraju treba izračunati pH-vrijednost:
Odgovor: pH-vrijednost navedene otopine je 2,72.
Na kraju…
Rješavanjem interaktivnih zadataka, usustavite pojmove obrađene u ovoj jedinici DOS-a te potom riješite i interaktivni kviz.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Koji je izraz za konstantu ionizacije (Kw) vode ispravno napisan:
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Ako se u otopinu kapne nekoliko kapi metiloranža otopina se oboji crveno.
Točna tvrdnja je:
Želite li pokušati ponovo?
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Koji je izraz za konstantu ionizacije vode ispravno napisan:
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Unesite odgovore na pripadajuća mjesta.
Klikom odaberite jedan točan odgovor.
Odaberite točan odgovor.
Ako se u otopinu kapne nekoliko kapi metiloranža otopina se oboji crveno. Točna tvrdnja je:
Želite li pokušati ponovo?