Kompleksni spojevi
Kompleksni spojevi
Alkalijskih i zemnoalkalijskih elemenata nema u elementarnom stanju zbog velike reaktivnosti.
Pojavljuju se u obliku različitih soli.
Ne možemo ih razlikovati po boji, jer su svi bijele boje.
Većina organskih spojeva je bijele boje.
Vrlo raznolike i intenzivne boje nalazimo kod spojeva prijelaznih elemenata.
Oni grade veliki broj kompleksnih spojeva.
Prijelazni elementi pripadaju d – bloku.
Posljednjim elektronima popunjavaju d-podljusku.
Uz pomoć PSE-a koji se nalazi u glavnom izborniku, napišite elektronske konfiguracije nekoliko prijelaznih elemenata.
Kompleksni spojevi
Alkalijski i zemnoalkalijski elementi u prirodi se ne nalaze u elementarnom stanju, jer su jako reaktivni, ali se pojavljuju u obliku različitih soli. Ne možemo ih razlikovati po boji, jer su sve bijele. Većina organskih spojeva također je bijele boje.
Međutim, vrlo raznolike i intenzivne boje nalazimo kod spojeva prijelaznih elemenata koji grade veliki broj kompleksnih spojeva.
Prijelazni elementi pripadaju d-bloku. Uz pomoć PSE-a kojem možete pristupiti u glavnom izborniku, napišite elektronske konfiguracije atoma nekoliko prijelaznih elemenata.
- Što je zajedničko elementima između 2. i 12. skupine PSE-a s obzirom na popunjenost d- podljuske?
- Mogu li prijelazni elementi otpuštanjem jednog ili dva elektrona s-podljuske zadnje ljuske postići elektronsku konfiguraciju plemenitog plina?
Odgovor:
- d-podljuska nije popunjena.
- Otpuštanjem elektrona zadnje ljuske mogu postići elektronsku konfiguraciju plemenitog plina.
Odgovorite na pitanja:
1. Što je zajedničko elementima između 2. i 12. skupine PSE-a s obzirom na popunjenost
d-podljuske?
2. Mogu li atomi prijelaznih elemenata otpuštanjem jednog ili dva elektrona s-podljuske zadnje ljuske postići elektronsku konfiguraciju plemenitog plina?
Odgovor:
1. Atomi elemenata između 2. do 12. skupine PSE-a nemaju popunjenu d-podljusku.
2. Atomi prijelaznih elemenata otpuštanjem jednog ili dva elektrona s-podljuske zadnje ljuske ne mogu postići elektronsku konfiguraciju plemenitog plina.
Istinitost tvrdnje provjerite tako da napišite elektronske konfiguracije atoma željeza te dvovalentnoga i trovalentnoga iona željeza.
Na takav način prijelazni elementi grade spojeve u kojima postižu elektronsku konfiguraciju plemenitog plina.
To se događa vezanjem određenog broja iona ili molekula, koje imaju nevezne elektronske parove.
Tako nastaje kompleksni spoj.
Svaki kompleksni spoj sastoji se od centralnog metalnog iona i liganada.
Centralni ion je obično metal iz grupe prijelaznih elemenata, s nepopunjenom zadnjom elektronskom ljuskom.
Ligandi su ioni ili molekule koji se vežu na centralni ion.
Vezanjem liganada popunjavaju se prazne ili polupopunjene s, p i d –orbitale .
Ligandi mogu biti:
- , , , ,
- ili molekule , , , .
Atomi prijelaznih elemenata grade spojeve u kojima postižu elektronsku konfiguraciju atoma plemenitih plinova vezanjem određenog broja iona ili molekula, koje imaju nevezne elektronske parove. Tako nastaje kompleksni spoj.
Svaki kompleksni spoj sastoji se od centralnog metalnog iona i liganada – iona ili molekula koji se vežu na centralni ion. Vezanjem liganada popunjavaju se prazne ili polupopunjene s, p i d –orbitale. Ligandi mogu biti: , , , ,
ili molekule: , , , .
Prikažite Lewisovom simbolikom strukturne formule navedenih čestica; , , , , , , , , .
Što je zajedničko navedenim česticama?
Na temelju Lewisovih strukturnih formula može se zaključiti da sve prikazane čestice imaju nevezne elektronske parove.
Centralni metalni ion naziva se elektron – akceptor jer prima elektrone od liganada.
Ligandi se nazivaju elektron-donori jer u vezu donose elektrone.
Veze između metalnog iona i liganada su: kovalentne, jednake duljine i jakosti.
Ligandi koji doniraju centralnom ionu jedan elektronski par nazivaju se monodentatni.
Bidentatni su donori dva elektronska para.
Polidentatni daju centralnom ionu više (>) od dva para elektrona.
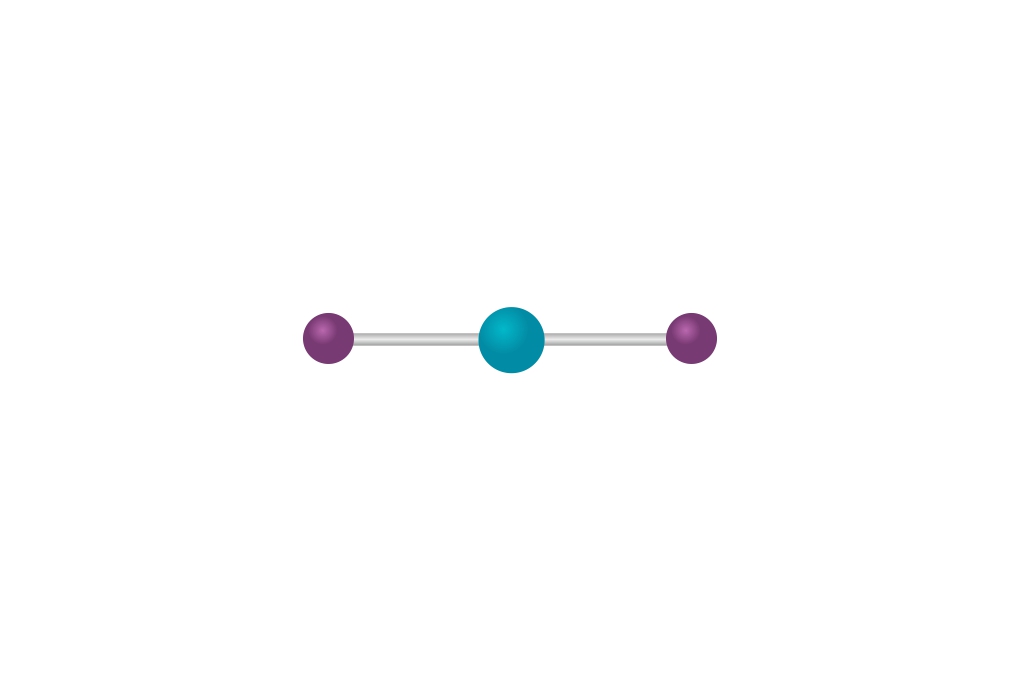
Koordinacijski broj je ukupan broj elektronskih parova kojima se centralni ion veže s ligandima.
Koordinacijski broj može biti u rasponu od 2 do 8.
Najmanje su zastupljeni neparni koordinacijski brojevi.
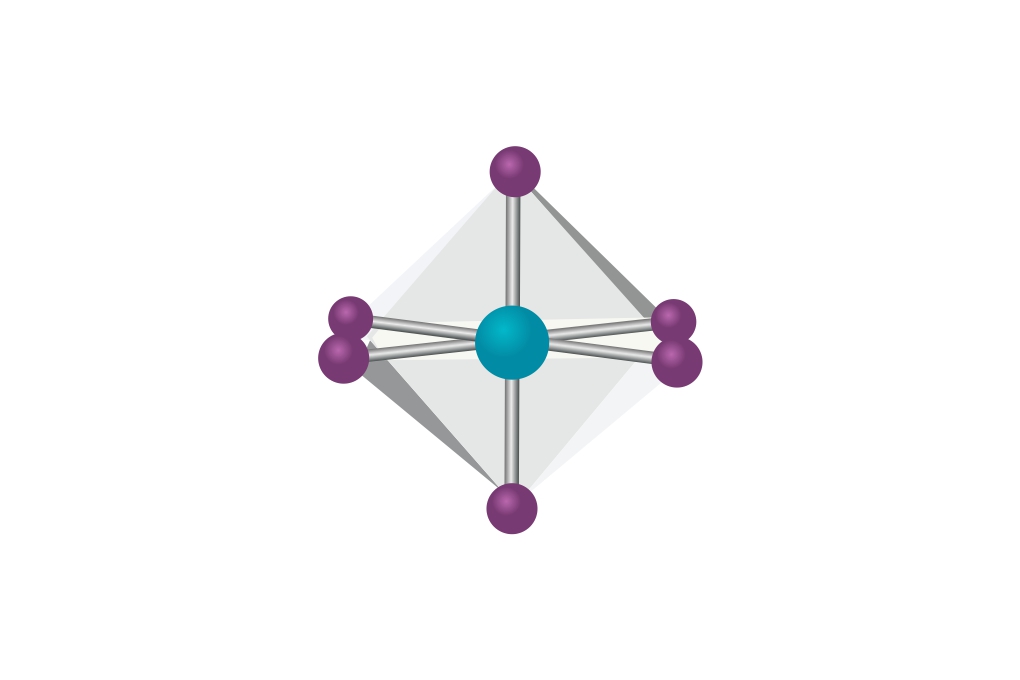
Od parnih koordinacijskih brojeva najčešći je koordinacijski broj 6.
Kompleksni ioni pišu se u uglatim zagradama [ ] .
Centralni metalni ion naziva se elektron-akceptor jer prima elektrone od liganada, koji se nazivaju elektron-donori jer u vezu donose elektrone.
Veze između metalnog iona i liganada su kovalentne, jednake duljine i jakosti. Ligandi koji doniraju centralnom ionu jedan elektronski par nazivaju se monodentatni, a ako doniraju dva elektronska para bidentatni ligandi. Polidentatni ligandi daju centralnom ionu više od dva para elektrona.
Ukupan broj elektronskih parova kojima se centralni ion veže s ligandima naziva se koordinacijski broj. Koordinacijski broj može biti u rasponu od dva do osam. Najmanje su zastupljeni neparni koordinacijski brojevi, a od parnih najčešći je koordinacijski broj šest. Formule kompleksnih iona pišu se u uglatim zagradama.
Unesite odgovore na pripadajuća mjesta.
Kompleksni spoj je neutralan, pa se u njemu mogu nalaziti anioni i kationi koji mogu, ali i ne moraju biti izravno vezani za centralni atom.
Na primjer: \ce{[Ag(NH3)2]Cl} \), \ce{K3[Fe(CN)6]} \), \ce{Na3[AlF6]} \).
Želite li pokušati ponovo?
Nacrtajte shematski zadnju ljusku atoma bakra () i kationa .
Lewisovom simbolikom prikažie molekulu amonijaka (NH3).
Koliko se molekula amonijaka () veže u kompleksni spoj da bi centralni ion bakra () imao elektronsku konfiguraciju najbližeg plemenitog plina?
Kation bakra () ima popunjenu treću ljusku.
Nacrtajte shematski zadnju ljusku atoma bakra i kationa . Lewisovom simbolikom prikažite strukturu molekule amonijaka. Koliko se molekula amonijaka veže u kompleksni spoj da bi centralni ion bakra imao elektronsku konfiguraciju najbližeg plemenitog plina?
Odgovor:
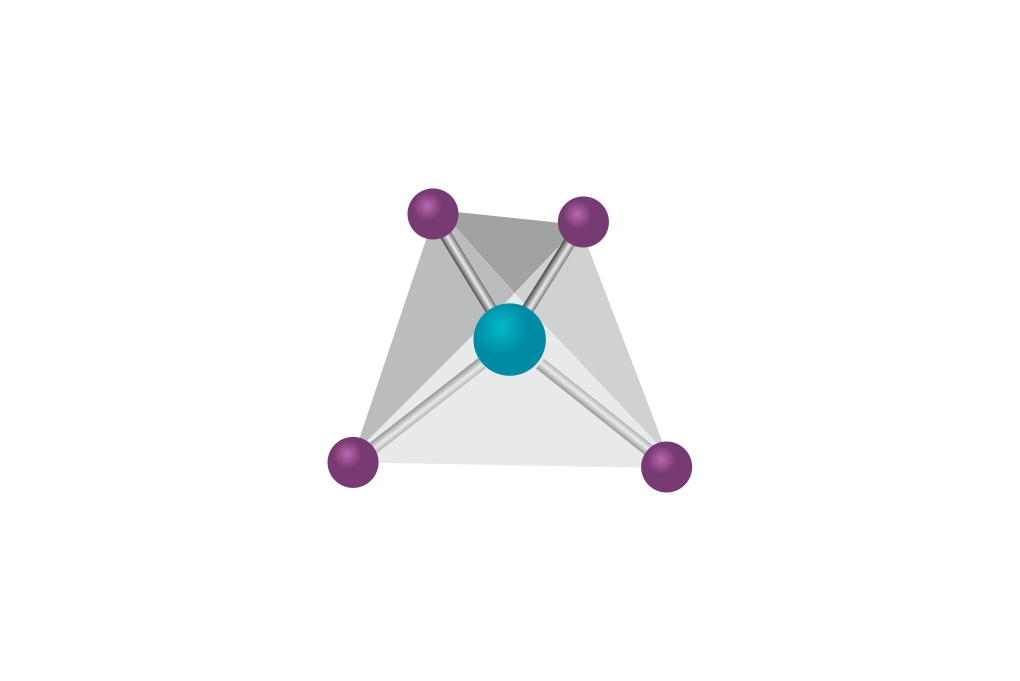
Kation bakra ima popunjenu treću ljusku. Vezanjem četiri molekule amonijaka koje doniraju četiri nevezna elektronska para u s- i p- podljuske četvrte ljuske postignuta je elektronska konfiguracija plemenitog plina kriptona.
Veliki broj metala tvori kompleksne spojeve. Apsorpcija elektromagnetskog zračenja, a time i boja kompleksnih spojeva posljedica je elektronske konfiguracije atoma prijelaznih metala. Raspored liganada može se odrediti uz pomoć VSEPR-modela.
Veliki broj metala tvori kompleksne spojeve.
Elektronska konfiguracija prijelaznih metala, nepopunjene d-orbitale određuju:
- apsorpciju elektromagnetskog zračenja određenih valnih duljina
- obojanost kompleksnih spojeva.
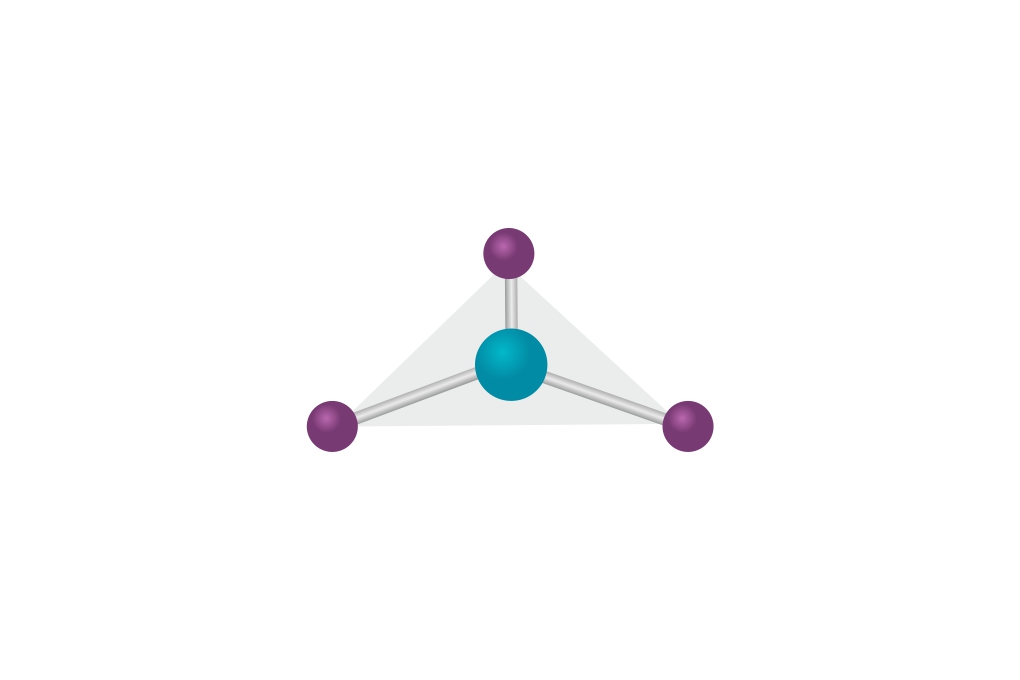
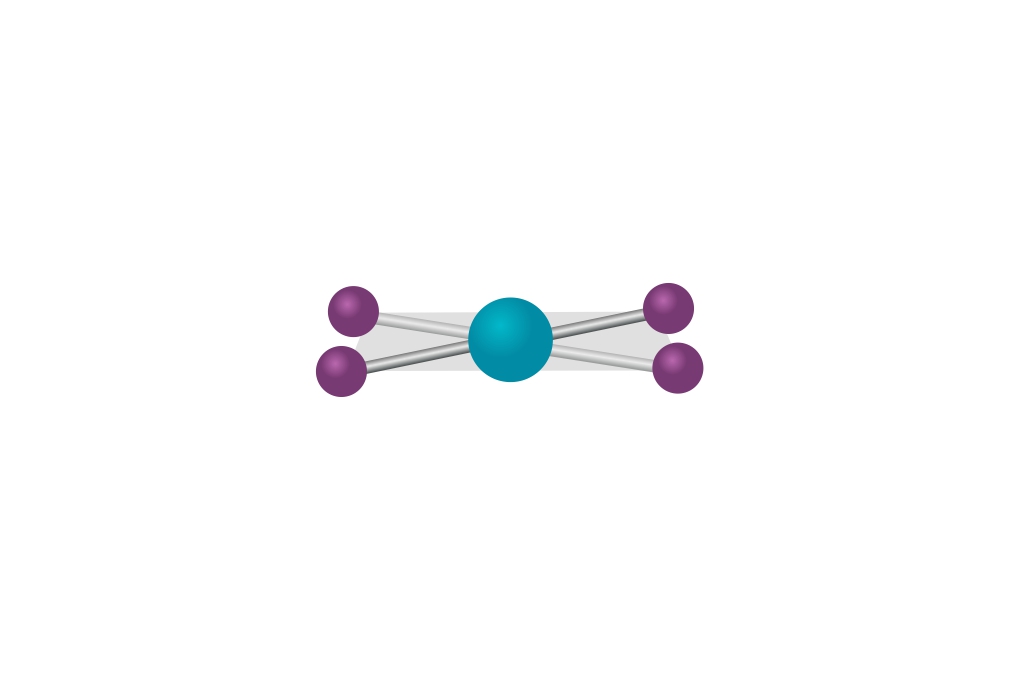
Raspored liganada može se odrediti uz pomoć VSEPR modela.
Mnogi kompleksni spojevi prijelaznih metala koriste se kao katalizatori u industriji.
Koriste se i kao katalizatori bioloških procesa.
Najpoznatiji među njima su:
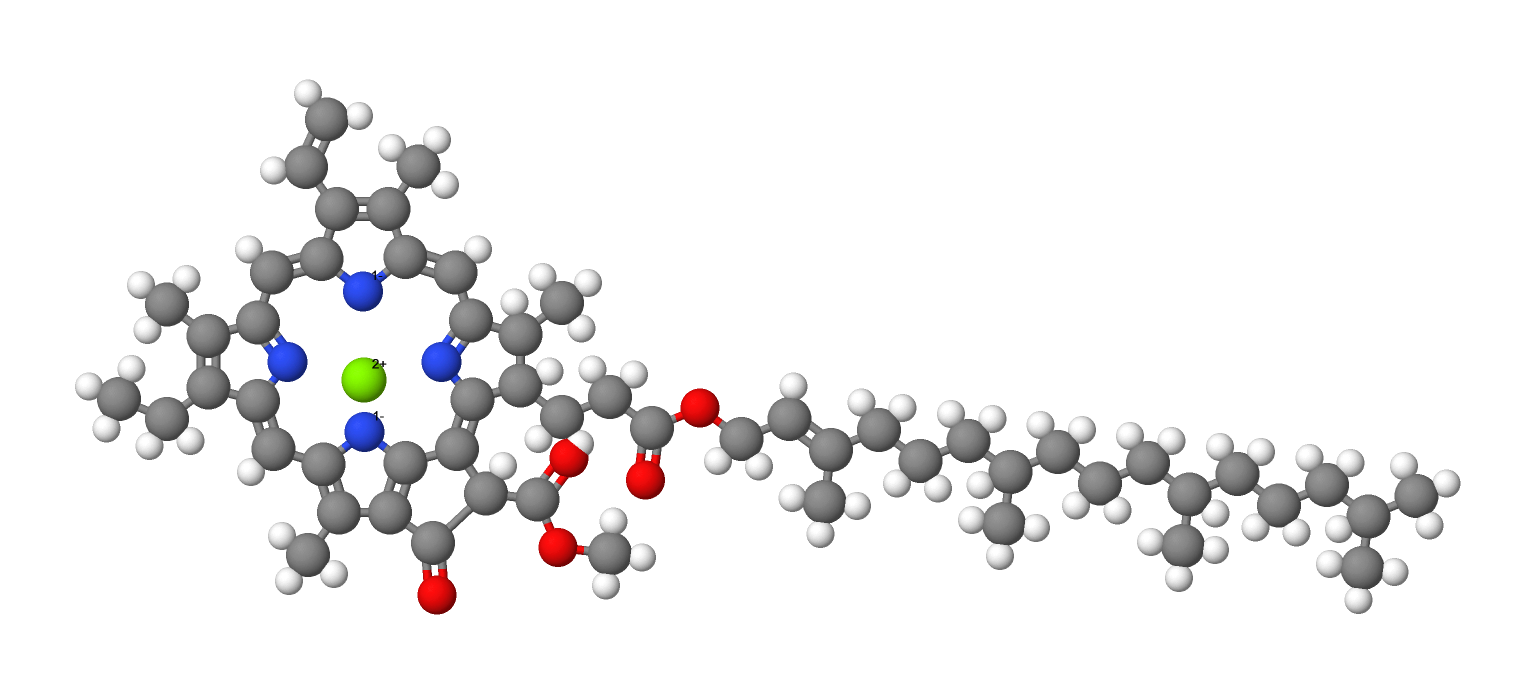
- a) klorofil (središnji ion je magnezijev kation)
- b) hem (središnji ion je željezov (II) kation).
Mnoge kompleksne spojeve prijelaznih metala koristi se kao katalizatore u industriji, ali su i katalizatori bioloških procesa. Najpoznatiji među njima je klorofil kod kojega je središnji ion magnezijev kation i hem kod kojega je središnji ion željezov(II) kation.